
Wetenschap
Wat is de molariteit van een oplossing die 93,5 g kaliumchloride bevat opgelost in een oplossing van 500 ml?
1. Bepaal de molaire massa kaliumchloride (KCL):
* Kalium (k) heeft een molaire massa van 39,10 g/mol
* Chloor (CL) heeft een molaire massa van 35,45 g/mol
* Molaire massa van KCl =39,10 g/mol + 35,45 g/mol =74,55 g/mol
2. Converteer de massa KCL naar mollen:
* Mol KCl =(massa KCl) / (molaire massa van KCl)
* Mol KCl =93,5 g / 74,55 g / mol =1,25 mol
3. Converteer het volume van de oplossing naar liters:
* Volume van oplossing =500 ml =0,5 L
4. Bereken de molariteit (M):
* Molariteit (m) =(mol opgeloste stof) / (volume van oplossing in liters)
* Molariteit (m) =1,25 mol / 0,5 l =2,5 m
Daarom is de molariteit van de kaliumchloride -oplossing 2,5 m.
 Fun Rainforest Science Experiments
Fun Rainforest Science Experiments Klimaatverandering keert een rivierstroom in Canadese gletsjer om
Klimaatverandering keert een rivierstroom in Canadese gletsjer om  Wetenschappers onderzoeken mysterieus smelten van aardkorst in het westen van Noord-Amerika
Wetenschappers onderzoeken mysterieus smelten van aardkorst in het westen van Noord-Amerika Studie identificeert belangrijke belemmeringen voor de financiering van een duurzame oceaaneconomie
Studie identificeert belangrijke belemmeringen voor de financiering van een duurzame oceaaneconomie Unilever halveert gebruik nieuw plastic
Unilever halveert gebruik nieuw plastic
Hoofdlijnen
- Wat is het potentieel om te inruilen in het concept van evolutionaire soorten?
- Wat is Clostridium anthracis?
- Welke twee kenmerken definiëren gymnospermen?
- Heeft iemand enig idee wat het OCR AS Biologie praktijkexamen in mei 2008 zal zijn?
- Nieuw onderzoek om uit te zoeken hoe microben rijstplanten beïnvloeden
- Hoe zeewiervretende krabben koraalriffen kunnen helpen redden
- Wanneer een oudercel verschillende kernen maakt en zich verdeelt om dochtercellen te maken?
- Onderzoek toont aan dat kapucijnapen stokken en stenen gebruiken om ondergronds naar voedsel te graven
- Hoeveel chromosomen heeft schimmels?
- Eenvoudige watertest kan verlammende botziekte voorkomen

- Nieuwe klasse katalysatoren voor energieconversie

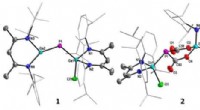
- Toekomstige opties voor het opslaan van koolstofdioxide:Synthese van anorganische heteroalkenen
- Deadlines voor het recyclen van kunststoffen dreigen - zullen bedrijven hun doelen bereiken?

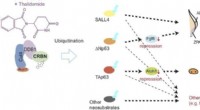
- Moleculaire basis van effecten van medicijnen op de ontwikkeling van ledematen en oren onthuld
 Omstreden Air France-KLM-aandelen stijgen als hotelgroep onderzoekt bod (update)
Omstreden Air France-KLM-aandelen stijgen als hotelgroep onderzoekt bod (update) Wat gebeurt er als de lamp blaast?
Wat gebeurt er als de lamp blaast?  Wat zou er met een snelheid gebeuren als positief werk op object werd gedaan?
Wat zou er met een snelheid gebeuren als positief werk op object werd gedaan?  Wat is een scroutum?
Wat is een scroutum?  Hoe we ontdekten dat de Britse schaliegasvoorraden minstens 80% kleiner zijn dan gedacht
Hoe we ontdekten dat de Britse schaliegasvoorraden minstens 80% kleiner zijn dan gedacht  Uit onderzoek blijkt dat door mannen gedomineerde MMA niet gunstig is voor gendergelijkheid
Uit onderzoek blijkt dat door mannen gedomineerde MMA niet gunstig is voor gendergelijkheid Een sterrenstelsel dat een abnormaal grote hoeveelheid energie uitzendt in de infrarood radio-ultraviolette en röntgenfuncties Elektromagnetisch spectrum staat bekend als een (n)?
Een sterrenstelsel dat een abnormaal grote hoeveelheid energie uitzendt in de infrarood radio-ultraviolette en röntgenfuncties Elektromagnetisch spectrum staat bekend als een (n)?  Kunnen de zon en de maan uit de lucht vallen?
Kunnen de zon en de maan uit de lucht vallen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

