
Wetenschap
Verwarming zinksulfide in de presentatie van zuurstof levert de na 2ZNS 3O2 --- 2Zno 2SO2 als 1,72 mol Zns wordt verwarmd 3,04 O2 welke reactant zal eerst worden opgebruikt?
1. Evenwichtige chemische vergelijking:
Je hebt de evenwichtige vergelijking al verstrekt:
2Zns + 3o₂ → 2Zno + 2So ₂
2. Mol -verhoudingen:
De evenwichtige vergelijking vertelt ons de molverhoudingen van reactanten en producten:
* 2 mol Zn's reageren met 3 mol O₂
3. Bereken mol O₂ nodig:
* Je hebt 1,72 mol Zn's.
* Om alle ZN's te gebruiken, zou u (1,72 mol Zns) * (3 mol O₂ / 2 mol Zns) nodig hebben =2,58 mol O₂
4. Vergelijk de mol O₂ nodig om mol te mollen beschikbaar:
* Je hebt 2,58 mol O₂ nodig
* Je hebt slechts 3,04 mol O₂
Conclusie:
Je hebt meer o₂ dan je nodig hebt om met alle ZN's te reageren. Daarom is zns de beperkende reactant en zal eerst worden opgebruikt.
 De grootste vulkaanuitbarsting van zwaveldioxide in 2018
De grootste vulkaanuitbarsting van zwaveldioxide in 2018 Hoe redden we bejaarde Australiërs van de hitte? Onze steden groener maken is een goed begin
Hoe redden we bejaarde Australiërs van de hitte? Onze steden groener maken is een goed begin Nieuwe methode onthult kleine microplastics in de subtropische oceaan van Japan
Nieuwe methode onthult kleine microplastics in de subtropische oceaan van Japan Atmosferische wetenschappers voeren veldexperimenten uit om windstroming over complex bergterrein te bestuderen
Atmosferische wetenschappers voeren veldexperimenten uit om windstroming over complex bergterrein te bestuderen Studie zegt dat koraalverbleking op het Great Barrier Reef niet beperkt is tot ondiepe diepten
Studie zegt dat koraalverbleking op het Great Barrier Reef niet beperkt is tot ondiepe diepten
Hoofdlijnen
- Mummies buikjes om de evolutie van de spijsvertering te onthullen
- Wat heeft de bijnaam de krachtpatser van de cel en die betrokken is bij de energieproductie voor cellen?
- Fagen een effectief alternatief voor het gebruik van antibiotica in de aquacultuur
- Wat is de fase in de mitose waarin het kernmembraan verdwijnt?
- Wat is animally -protist pseudopoden?
- Welke term verwijst naar de vorm van een bacterie?
- Beschrijf hoe veranderingen in het milieu gedragsfysiologische morfologische of adaptieve reacties in organismen kunnen veroorzaken?
- Hoe zijn modellen nuttig voor wetenschappers?
- Wat bevat je botten die rode bloedcellen maakt?
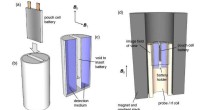
- Chemici ontwikkelen MRI-achtige techniek om te detecteren wat er aan de hand is met batterijen
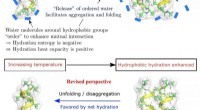
- Vouwende eiwitten voelen de hitte, en koud
- Chemicus maakt de volgende generatie neurowetenschappelijke tools

- Chemici maken cellulaire krachten zichtbaar op moleculaire schaal
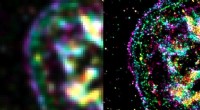
- Detectie van ethyleen, het fruitrijpingshormoon

 In het belang van de planeet, koeltechniek heeft een update nodig
In het belang van de planeet, koeltechniek heeft een update nodig De minst bruikbare vorm van energie is?
De minst bruikbare vorm van energie is?  Sally doordrenkt het zuidoosten van de VS nadat ze de Golfkust als orkaan heeft geraakt
Sally doordrenkt het zuidoosten van de VS nadat ze de Golfkust als orkaan heeft geraakt Wat zijn de belangrijkste lichamen die een ster om een ster omdraaien?
Wat zijn de belangrijkste lichamen die een ster om een ster omdraaien?  Wat zou het einde kunnen resulteren in het terrestrische en aquatische ecosysteem als alle ontleders, inclusief slijmvormen, water niet langer bestonden?
Wat zou het einde kunnen resulteren in het terrestrische en aquatische ecosysteem als alle ontleders, inclusief slijmvormen, water niet langer bestonden?  NASA kijkt naar regen in het Midwesten en smeltende sneeuw die hebben bijgedragen aan overstromingen
NASA kijkt naar regen in het Midwesten en smeltende sneeuw die hebben bijgedragen aan overstromingen Waarom zou de impact van een zware steengolven met een hogere amplitude produceren dan lichte steen zou doen?
Waarom zou de impact van een zware steengolven met een hogere amplitude produceren dan lichte steen zou doen?  Scavengers of the Tundra
Scavengers of the Tundra
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

