
Wetenschap
Waarom vormt boor elektronefonische verbinding?
1. Elektronische configuratie:
* Boron heeft drie valentie -elektronen (2s² 2p¹).
* Om een stabiel octet te bereiken, heeft het nog vijf elektronen nodig.
2. Bonding:
* Boor geeft er de voorkeur aan om covalente bindingen te vormen en deelt elektronen met andere atomen.
* Het kan echter slechts drie covalente bindingen vormen vanwege zijn beperkte valentie -elektronen.
* Dit laat het achter met slechts zes elektronen in de valentieschil, twee elektronen kort van een octet.
3. Elektroneficiëntie:
* De resulterende verbinding wordt een elektron-deficiënte verbinding genoemd .
* Deze verbindingen missen de volledige aanvulling van elektronen die nodig zijn voor een stabiel octet.
4. De rol van lege orbitalen:
* Boron kan zijn lege 2P -orbitaal gebruiken om elektronen uit aangrenzende atomen te accepteren.
* Dit helpt om de elektroneficiëntie te compenseren, maar niet volledig.
* Dit resulteert in sterke bindingen met een hoog covalente karakter, maar creëert ook een hoge elektronenvraag in de verbinding.
Voorbeelden:
* borane (bh₃): Het heeft slechts zes valentie-elektronen rond het booratoom, waardoor het elektron-deficiënt is. Het accepteert gemakkelijk elektronen uit andere moleculen en vormt adducten.
* diborane (b₂h₆): Het is een klassiek voorbeeld van een elektron-deficiënte verbinding. Het heeft drie-center twee-elektronenbindingen (3C-2E) waar twee booratomen een paar elektronen delen met een overbrugging waterstofatoom. Dit zorgt voor de vorming van stabiele bindingen, ondanks de elektroneficiëntie.
gevolgen van elektroneficiëntie:
* Hoge reactiviteit: Elektron-deficiënte verbindingen zijn zeer reactief vanwege hun sterke elektronenvraag.
* Lewis -zuurgraad: Ze accepteren gemakkelijk elektronenparen en fungeren als Lewis -zuren.
* ongebruikelijke structuren: Ze nemen vaak ongebruikelijke structuren aan om elektroneficiëntie te minimaliseren, zoals de overbruggende waterstofatomen in diboraan.
Samenvattend: Borons beperkte valentie-elektronen en de noodzaak om een stabiel octet te bereiken leiden tot de vorming van elektron-deficiënte verbindingen. Deze verbindingen worden gekenmerkt door hun sterke elektronenvraag, hoge reactiviteit en Lewis -zuurgraad.
 De relatieve luchtvochtigheid bepalen met een natte en droge bolthermometer
De relatieve luchtvochtigheid bepalen met een natte en droge bolthermometer Plantaardig materiaal recyclen tot voorraadchemicaliën met elektrochemie
Plantaardig materiaal recyclen tot voorraadchemicaliën met elektrochemie Wat betekent chemische volatiliteit op het veiligheidsgegevensblad?
Wat betekent chemische volatiliteit op het veiligheidsgegevensblad?  Wat is een stof die het chemische proces versnelt?
Wat is een stof die het chemische proces versnelt?  Hoe kunnen ionen worden beschreven?
Hoe kunnen ionen worden beschreven?
Hoofdlijnen
- Wat is de wetenschappelijke naam voor werk?
- Cloverleaf -structuur heeft mRNA -tRNA of rRNA?
- Hoe de kern vormt een pollenkorrel die een vrouwelijke eiercel bemoeilijkt?
- Glucose en geen andere suiker wordt in cellen getransporteerd door eiwitdragermoleculen in het celoppervlakmembraan. Hoe herkent Glucose specifiek?
- Waarom dieren hun eigen geslacht het hof maken
- Wat is wetenschappelijke evolutie?
- Welk idee van gebaseerd op fossielen en het moderne organisme dat hij in feite heeft gevonden, zegt in feite dat generieke veranderingen door latere generaties worden geërfd?
- Varens krijgen eindelijk een genoom en onthullen een geschiedenis van DNA-hamsteren en kleptomanie
- Producten vervaardigd door Anaerobe Ademhaling
- Onderzoekers ontdekken een nieuwe route om complexe kristallen te vormen

- Nieuwe klasse katalysatoren voor energieconversie

- Nieuw waargenomen eenwaardige calciumionen vertonen onverwachte metaalachtigheid en ferromagnetisme
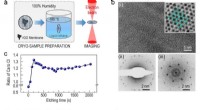
- Uitdagingen bij de ontwikkeling van elektrokatalysatoren

- Etherische oliën herstellen de effectiviteit van insecticiden tegen bedwantsen

 Wat is een voorbeeld van object dat beweegt met constante snelheid en snelheid?
Wat is een voorbeeld van object dat beweegt met constante snelheid en snelheid?  4 basisbehoeften voor een organisme?
4 basisbehoeften voor een organisme?  Bezorging ruimtestation uit Virginia op het laatste moment mislukt
Bezorging ruimtestation uit Virginia op het laatste moment mislukt Wat is een uitgebalanceerde chemische vergelijking voor calciumnitraat en natriumsulfaat?
Wat is een uitgebalanceerde chemische vergelijking voor calciumnitraat en natriumsulfaat?  Hoeveel bindingen vormen de koolstofatomen met elkaar in het C2H2-molecuul?
Hoeveel bindingen vormen de koolstofatomen met elkaar in het C2H2-molecuul?  Koude lucht stijgt op - wat dat betekent voor het klimaat op aarde
Koude lucht stijgt op - wat dat betekent voor het klimaat op aarde Waarom wordt weinig warmte vastgehouden in de warme thermosfeer?
Waarom wordt weinig warmte vastgehouden in de warme thermosfeer?  Wat zou de zwaartekracht op een blok van 1 kg zijn?
Wat zou de zwaartekracht op een blok van 1 kg zijn?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

