
Wetenschap
Wat is de empirische formule van een koolwaterstof met 85,7 procent koolstof en 14,3 waterstof?
1. Neem een monster van 100 gram aan:
* Dit maakt de berekeningen eenvoudiger, omdat de percentages zich direct vertalen naar gram.
* 85,7 gram koolstof (c)
* 14.3 gram waterstof (H)
2. Converteer grams naar mollen:
* Verdeel de massa van elk element door zijn molaire massa:
* Koolstof:85,7 g / 12.01 g / mol =7,14 mol
* Waterstof:14,3 g / 1.01 g / mol =14,16 mol
3. Zoek de eenvoudigste gehele getalverhouding:
* Verdeel elke molwaarde door de kleinste molwaarde (7.14 mol in dit geval):
* Koolstof:7.14 mol / 7.14 mol =1
* Waterstof:14.16 mol / 7.14 mol =2
4. Schrijf de empirische formule:
* De empirische formule is de eenvoudigste verhouding van het hele nummer van atomen in een verbinding.
* De empirische formule van deze koolwaterstof is ch₂ .
 Vorm geven aan de manier waarop de vervormbaarheid van rode bloedcellen wordt beoordeeld:onderzoekers ontwikkelen een nieuwe aanpak
Vorm geven aan de manier waarop de vervormbaarheid van rode bloedcellen wordt beoordeeld:onderzoekers ontwikkelen een nieuwe aanpak  Wat zijn de onderdelen voor een atoom?
Wat zijn de onderdelen voor een atoom?  Video:Waarom limoensap je huid verbrandt in de zon
Video:Waarom limoensap je huid verbrandt in de zon Wat is de chemische vergelijking voor sojalecithine?
Wat is de chemische vergelijking voor sojalecithine?  Mariene bacterie werpt licht op beheersing van giftige metalen
Mariene bacterie werpt licht op beheersing van giftige metalen
 NASA's TROPICS Pathfinder-satelliet produceert wereldwijde beelden van het eerste licht en legt orkaan Ida . vast
NASA's TROPICS Pathfinder-satelliet produceert wereldwijde beelden van het eerste licht en legt orkaan Ida . vast Waarom is het geleidelijke verlies van regenwouden een belangrijke zorg voor het milieu?
Waarom is het geleidelijke verlies van regenwouden een belangrijke zorg voor het milieu?  Moskou geeft groen licht aan Yamal gas super project
Moskou geeft groen licht aan Yamal gas super project Globale analyse van onderzeese canyons kan licht werpen op Marslandschappen
Globale analyse van onderzeese canyons kan licht werpen op Marslandschappen Wat wordt een feit verkregen door het gebruik van zintuigen?
Wat wordt een feit verkregen door het gebruik van zintuigen?
Hoofdlijnen
- Noem het weefsel dat sucrose transporteert?
- Cellulaire ademhaling gebruikt 1 molecuul glucose om wat te produceren?
- Onderzoek laat zien hoe cellen grote genen verwerken
- Wetenschappers onderzoeken hoe vrouwen hun tweede X-chromosoom afsluiten
- Drie manieren waarop genetische diversiteit optreedt tijdens meiose
- Een klier die scheidt door kanalen?
- Waarom werken alle orgelsystemen met elkaar?
- Klimaatverandering, bevolkingsgroei kan leiden tot aquacultuur in open oceaan
- Sumatraanse neushoorns zijn nooit hersteld van verliezen tijdens het Pleistoceen, genoom bewijs toont
- Onderzoekers ontwikkelen nieuwe methode voor levering van glucagon

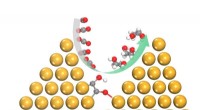
- Superselectieve katalysatoren sleutel tot koolstofconversie
- Evaluatie van nieuwe verwerkingsplatforms voor farmaceutische productie

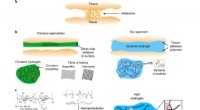
- Onderzoekers ontdekken dat gel littekenweefsel vermindert na operatie bij dieren
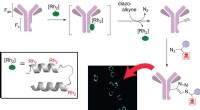
- Metaal vereenvoudigt de synthese van antilichaamgeneesmiddelen
 Welke ingredzaamheid is er in water?
Welke ingredzaamheid is er in water?  Hoeveel ton in 10063 bbl diesel?
Hoeveel ton in 10063 bbl diesel?  Het binnenste van de aarde slikt meer koolstof op dan gedacht
Het binnenste van de aarde slikt meer koolstof op dan gedacht Alaska vulkaan Q&A:uitbarstingen hebben hoogvliegende gevolgen
Alaska vulkaan Q&A:uitbarstingen hebben hoogvliegende gevolgen Wanneer energie wordt omgezet van de ene vorm naar de andere in het lichaam die is verloren?
Wanneer energie wordt omgezet van de ene vorm naar de andere in het lichaam die is verloren?  Is er een space shuttle geland op planeten?
Is er een space shuttle geland op planeten?  Vermogen stroma gassen zoals koolstofdioxide en zuurstof tussen de plantenatmosfeer toe?
Vermogen stroma gassen zoals koolstofdioxide en zuurstof tussen de plantenatmosfeer toe?  Hoe gaan andere moleculen door het selectief permeabele celmembraan?
Hoe gaan andere moleculen door het selectief permeabele celmembraan?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

