
Wetenschap
Wat is de depressie van het vriespunt van een waterige oplossing die magnesiumchloride van 25,0 gram bevat?
1. Bereken de molaliteit van de oplossing.
* Molaire massa van mgcl₂: 24.31 g/mol (mg) + 2 * 35,45 g/mol (CL) =95,21 g/mol
* mol mgcl₂: 25,0 g / 95,21 g / mol =0,263 mol
* Mass van water (oplosmiddel): Stel dat u een oplossing van 1 kg (1000 g) maakt. Daarom is de massa water 1000 g - 25,0 g =975 g =0,975 kg
* molaliteit (m): mol opgeloste stof / kg oplosmiddel =0,263 mol / 0,975 kg =0,270 mol / kg
2. Bereken de Van't Hoff -factor (i).
* mgcl₂ dissocieert in 3 ionen in oplossing:mg²⁺ + 2cl⁻. Daarom i =3.
3. Bereken de depressie van het vriespunt (Δt f ).
* Freezing Point Depression Constant (K F ) voor water: 1,86 ° C/m
* Δt f =i * k f * M
* Δt f =3 * 1,86 ° C/m * 0,270 m =1,50 ° C
Daarom is het vriespuntdepressie van de waterige oplossing die 25,0 gram magnesiumchloride bevat 1,50 ° C.
Belangrijke opmerking: Deze berekening veronderstelt ideaal gedrag, wat betekent dat de opgeloste stof volledig in ionen dissocieert. In werkelijkheid kan er wat ionenparen optreden, wat de werkelijke invriezende puntdepressie enigszins zou verminderen.
 Bliksemstormen minder waarschijnlijk in een opwarmende planeet, studie suggereert:
Bliksemstormen minder waarschijnlijk in een opwarmende planeet, studie suggereert: Kunnen geografische barrières de vorming van nieuwe soorten garanderen?
Kunnen geografische barrières de vorming van nieuwe soorten garanderen?  Hoeveel water houden snowpacks vast? Een betere manier om de vraag te beantwoorden
Hoeveel water houden snowpacks vast? Een betere manier om de vraag te beantwoorden Hoe wordt Photochemical Smog gevormd?
Hoe wordt Photochemical Smog gevormd?  Wat ontbreekt er in de projecties van bossterfte? Een kijkje onder de grond
Wat ontbreekt er in de projecties van bossterfte? Een kijkje onder de grond
Hoofdlijnen
- Wat voor soort wortel heeft een tomatenplant?
- Hoe bestudeer je gezichtsvertekeningen zonder vooroordelen?
- Wat zijn de overeenkomsten tussen een parameciumcel en elodea -cel?
- Hoe reageren mannen en vrouwen op gendervooroordelen in STEM?
- Welke organen zijn bekleed met al het slijmvlies?
- Reconstructie van ijstijddiëten onthult ontrafelend levensweb
- Wetenschappers ontcijferen hoe planten zonnebrand voorkomen
- Welke communicerende resultaten van een onderzoek laten andere wetenschappers toe?
- Onderzoekers creëren een nauwkeuriger model van hoe sommige microben naar voedingsstoffen zoeken
- Chemische reacties zien met muziek

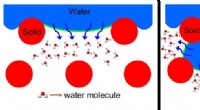
- Wetenschappers onthullen belangrijke inzichten in opkomende waterzuiveringstechnologie
- Chemici ontwikkelen contaminantendetectietechniek voor heparine

- Test op levensbedreigend voedingstekort wordt gemaakt van ingewanden van bacteriën

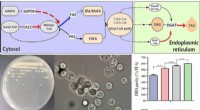
- Celfabriek die zeer zuiver DHA kan produceren
 Wat is een echt voorbeeld van sintelkegelvulkaan?
Wat is een echt voorbeeld van sintelkegelvulkaan?  Hoeveel protonen, nuetronen en elektronen zitten er in 162Gd plus 3?
Hoeveel protonen, nuetronen en elektronen zitten er in 162Gd plus 3?  Welk deel van het blad bevatte zetmeel?
Welk deel van het blad bevatte zetmeel?  Wanneer stoffen mengen maar niet binden wordt gebeld hoe?
Wanneer stoffen mengen maar niet binden wordt gebeld hoe?  Hoe is het menselijke genoomproject gerelateerd aan gentherapie?
Hoe is het menselijke genoomproject gerelateerd aan gentherapie?  Wat zijn veronderstellingen die wetenschappers maken over de natuurlijke wereld?
Wat zijn veronderstellingen die wetenschappers maken over de natuurlijke wereld?  Hoe kan het kruipen van de energiemeter verminderen?
Hoe kan het kruipen van de energiemeter verminderen?  Door de mens gemaakt universum binnenkort beschikbaar?
Door de mens gemaakt universum binnenkort beschikbaar?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

