
Wetenschap
Oplossingen gekenmerkt door de vorming van hydroxide -ionen oh zijn?
Dit is waarom:
* pH -schaal: De pH -schaal meet de zuurgraad of alkaliteit van een oplossing. Een pH van 7 is neutraal. Waarden onder de 7 zijn zuur en waarden boven 7 zijn basic (alkalisch).
* Hydroxide -ionen: Hydroxide-ionen (OH-) zijn verantwoordelijk voor de alkaliteit van een oplossing. Hoe hoger de concentratie van hydroxide -ionen, hoe meer fundamenteel de oplossing.
* waterstofionen: Omgekeerd hebben zure oplossingen een hogere concentratie waterstofionen (H+).
Voorbeelden van basisoplossingen:
* Natriumhydroxide (NaOH) :Algemeen bekend als loog, het is een sterke basis die volledig in water dissocieert om hydroxide -ionen te produceren.
* kaliumhydroxide (KOH): Net als natriumhydroxide is het een andere sterke basis.
* ammoniak (NH3): Dit is een zwakke basis die reageert met water om hydroxide -ionen te vormen.
Belangrijke opmerking: De vorming van hydroxide-ionen (OH-) is een belangrijk kenmerk van basisoplossingen, maar niet alle basisoplossingen vormen deze rechtstreeks. Sommige bases reageren met water om hydroxide -ionen te produceren.
 Nieuwe polymeren vertonen interactie met cellen
Nieuwe polymeren vertonen interactie met cellen  Toekomstige legervoertuigen zouden een verbetering in structurele materialen kunnen zien
Toekomstige legervoertuigen zouden een verbetering in structurele materialen kunnen zien Substantie wiens kleinste eenheid bestaat uit meer dan één element en kan niet worden gescheiden?
Substantie wiens kleinste eenheid bestaat uit meer dan één element en kan niet worden gescheiden?  Wat is de moleculaire formule van kaliumzincaat?
Wat is de moleculaire formule van kaliumzincaat?  Wat heeft de meeste atomen één mol gouden helium of lood?
Wat heeft de meeste atomen één mol gouden helium of lood?
 Nieuwe studie toont aan dat olieramp Deepwater Horizon groter is dan eerder werd gedacht
Nieuwe studie toont aan dat olieramp Deepwater Horizon groter is dan eerder werd gedacht Waarom hebben planten mineraal nodig?
Waarom hebben planten mineraal nodig?  Het herstel in Florida komt in een stroomversnelling maar gevaren blijven bestaan
Het herstel in Florida komt in een stroomversnelling maar gevaren blijven bestaan Ellende, onzekerheid nadat Irma de idylle van Florida bereikt
Ellende, onzekerheid nadat Irma de idylle van Florida bereikt Antarctische gletsjers kwetsbaar voor stijgende temperaturen
Antarctische gletsjers kwetsbaar voor stijgende temperaturen
Hoofdlijnen
- Wat zijn therapeutische eiwitten?
- Hoe verhoudt het scheppingsverhaal zich tot de celtheorie?
- Wat is het laatste nieuws over de darmflora? Concordia-studenten microbiologie publiceren hun bevindingen
- Wat is een biologische catalist?
- Waarom hebben cellen fosfor nodig?
- Wat is en niet wetenschap?
- Welke verklaring geeft het beste een basiswetenschappelijke veronderstelling uit?
- Waarom zijn modellen nuttig bij het bestuderen van wetenschappelijke concepten?
- Wat zijn de bouwstenen voor eiwitten?
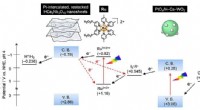
- Nieuwe fotokatalysator verhoogt de efficiëntie van watersplitsing voor schone waterstofproductie
- Duurzame scheidingstechnologie maakt nieuwe toepassingen mogelijk

- Niet-kloneerbare tag bestrijdt vervalsers

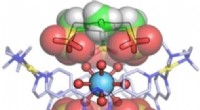
- Kooi met doppen:selectieve opsluiting van hydraten van zeldzame aardmetalen in gastheermoleculen
- De inkt van de toekomst in gedrukte elektronica

 Grafeenlagen verminderen slijtage en wrijving op glijdende stalen oppervlakken aanzienlijk
Grafeenlagen verminderen slijtage en wrijving op glijdende stalen oppervlakken aanzienlijk Cell on a chip onthult eiwitgedrag
Cell on a chip onthult eiwitgedrag Een veelbelovende combinatie:wetenschappers demonstreren nieuwe combinatie van materialen voor de kwantumwetenschap
Een veelbelovende combinatie:wetenschappers demonstreren nieuwe combinatie van materialen voor de kwantumwetenschap  Video:Nieuwe weersatelliet onderweg naar lancering
Video:Nieuwe weersatelliet onderweg naar lancering Is de eenheid megawatt-dag een energie-eenheid?
Is de eenheid megawatt-dag een energie-eenheid?  Veranderingen in steenwerktuigen kunnen laten zien hoe Mesolithische jager-verzamelaars reageerden op het veranderende klimaat
Veranderingen in steenwerktuigen kunnen laten zien hoe Mesolithische jager-verzamelaars reageerden op het veranderende klimaat  Wanneer realiseerde Newton zich dat de planeten rond de zon gaan?
Wanneer realiseerde Newton zich dat de planeten rond de zon gaan?  Wat gebeurt er als u soldiumchloride mengt met water?
Wat gebeurt er als u soldiumchloride mengt met water?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

