
Wetenschap
Kunnen kalium en zwavel een ionische verbinding vormen?
* kalium (k) is een metaal en metalen verliezen de neiging elektronen te verliezen om positief geladen ionen (kationen) te vormen. Kalium heeft één valentie -elektron en verliest het gemakkelijk om K⁺ te vormen.
* zwavel (s) is een niet -metaal en niet -metalen hebben de neiging om elektronen te krijgen om negatief geladen ionen (anionen) te vormen. Zwavel heeft zes valentie -elektronen en heeft er nog twee nodig om zijn octet te voltooien. Het krijgt twee elektronen om S²⁻ te vormen.
Wanneer kalium en zwavel reageren, doneren kaliumatomen hun elektronen aan zwavelatomen, waardoor een ionische binding wordt gevormd. De resulterende verbinding is kaliumsulfide (k₂s) .
De formule k₂s vertegenwoordigt het volgende:
* Twee kaliumionen (k⁺) voor elk sulfide -ion (s²⁻) om de ladingen in evenwicht te brengen.
* De algehele lading van de verbinding is neutraal.
Sleutelpunten:
* Ionische verbindingen worden gevormd tussen metalen en niet -metalen.
* De elektrostatische aantrekkingskracht tussen tegengesteld geladen ionen houdt de verbinding bij elkaar.
* De chemische formule van een ionische verbinding weerspiegelt de verhouding tussen kationen en anionen die nodig zijn om neutraliteit te bereiken.
 Waarom worden primair alkylhalogenide niet gesyntesiseerd met behulp van SN1 -reactie?
Waarom worden primair alkylhalogenide niet gesyntesiseerd met behulp van SN1 -reactie?  Hoe beïnvloedt het mengen van een vaste stof en vloeistof de totale mengmassa?
Hoe beïnvloedt het mengen van een vaste stof en vloeistof de totale mengmassa?  Wat is de edelgasnotatie van BK?
Wat is de edelgasnotatie van BK?  Wat is het eindproduct van Uranium 238?
Wat is het eindproduct van Uranium 238?  Wetenschappers onthullen rutheniumkatalysator voor het ontdekken en optimaliseren van nieuwe reacties
Wetenschappers onthullen rutheniumkatalysator voor het ontdekken en optimaliseren van nieuwe reacties
Hoofdlijnen
- Hoe noem je een plant die voedsel voor zichzelf maakt?
- DNA-ontdekking kan licht werpen op zeldzame kinderziekte
- Hoe nitraat de genexpressie in peulvruchten reguleert
- Beschrijf hoe eukaryotische cellen chromosomen veranderen als een cel zich voorbereidt op het delen van wat is het voordelig pakket -DNA voor deling?
- Freeze frame:Onderzoekers lossen op hoe cellen eiwitten ontvouwen
- Wie zijn een Filipijnse wetenschapper en wat hun bijdrage aan de vooruitgang van de fysieke wetenschap?
- Wat als je lichaam groeit omdat cellen wat doen?
- Wetenschappers ontdekken dat de meeste blauwe vinvissen rechtshandig zijn, behalve wanneer ze omhoog zwemmen
- Ik ben hetzelfde experiment dat geldt voor de F1-generatieA) ze zijn allemaal heterozygootB)Alles homozygootC)Alles zal wit zijn Kleur bloemD) Zuivere kweekE) Geen hierboven?
- Nieuw antibioticum verslaat bacteriële resistentie
- Synthese van een zeldzaam metaalcomplex van lachgas opent nieuwe perspectieven voor
- Ontziltingsonderzoek kan ingenieurs helpen om efficiënter schoon water te produceren
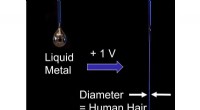
- Beheersing van stromen vloeibaar metaal bij kamertemperatuur
- Polymeercoating koelt gebouwen af

 Waarom beweegt de vloeistof in een thermometer?
Waarom beweegt de vloeistof in een thermometer?  Nieuwe protonenstarter voor optogenetica
Nieuwe protonenstarter voor optogenetica Wat is een orbitale hoogtepunt?
Wat is een orbitale hoogtepunt?  Astronomen ontdekten onlangs een maan die geen planeet rondomplan?
Astronomen ontdekten onlangs een maan die geen planeet rondomplan?  Hoe de spiraallengte te berekenen
Hoe de spiraallengte te berekenen  Welke sedimetaire rots heeft de kleinste korrelgrootte?
Welke sedimetaire rots heeft de kleinste korrelgrootte?  Wat kunnen deeltjes in een vloeistof doen?
Wat kunnen deeltjes in een vloeistof doen?  Onderzoek op nanoschaal zou betere manieren kunnen opleveren om kwaadaardige cellen te identificeren en te volgen
Onderzoek op nanoschaal zou betere manieren kunnen opleveren om kwaadaardige cellen te identificeren en te volgen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

