
Wetenschap
Hoeveel gram water wordt gevormd in 1 mol propanal brandwonden?
Hier leest u hoe u de grammen van water gevormd bent wanneer 1 mol propanal brandt:
1. Schrijf de gebalanceerde chemische vergelijking:
De verbranding van propanal (C₃h₆o) produceert koolstofdioxide (CO₂) en water (H₂o):
C₃h₆o + 4o₂ → 3co₂ + 3h₂o
2. Bepaal de molverhouding van water en propanal:
Uit de evenwichtige vergelijking zien we dat 1 mol propanal (c₃h₆o) 3 mol water produceert (H₂o).
3. Converteer mol water om te grammen:
* De molaire watermassa (H₂o) is 18.015 g/mol.
* Met behulp van de molverhouding en de molaire massa water:
3 mol H₂o × 18.015 g/mol =54.045 g h₂o
Daarom worden 54.045 gram water gevormd wanneer 1 mol propanal brandwonden.
 Vluchten wereldwijd lopen verhoogd risico op ernstige turbulentie als gevolg van klimaatverandering
Vluchten wereldwijd lopen verhoogd risico op ernstige turbulentie als gevolg van klimaatverandering NASA vindt nieuwe tropische storm Nana versterking in het Caribisch gebied
NASA vindt nieuwe tropische storm Nana versterking in het Caribisch gebied Slapende reus kan een einde maken aan het leven in de diepe oceaan
Slapende reus kan een einde maken aan het leven in de diepe oceaan Krachtige aardbeving wekt mensen uit hun slaap in Zuid-Filippijnen
Krachtige aardbeving wekt mensen uit hun slaap in Zuid-Filippijnen Bossen hielden hun adem in tijdens de onderbreking van de opwarming van de aarde, uit onderzoek blijkt
Bossen hielden hun adem in tijdens de onderbreking van de opwarming van de aarde, uit onderzoek blijkt
Hoofdlijnen
- Hoe worden xx chromosomen genoemd?
- Burn-out eist zware financiële tol van diergeneeskunde
- Waarom verlaten zoveel vrouwen de biologie?
- Gebruik van microscopen in de wetenschap
- San Diego Zoo pinguïn voorzien van orthopedisch schoeisel (update)
- Hoe boeren gebruik maken van wetenschappelijke vooruitgang om zoveel mogelijk biomassa te produceren?
- Welk bouwsteen is het belangrijkste structurele materiaal van organismen?
- Waar kwam de wetenschappelijke naam van konijn vandaan?
- Welke categorie macromoleculen zijn enzymen geclassificeerd?
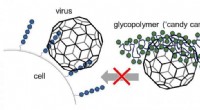
- Kunstmatige zuurstokken om virussen te blokkeren
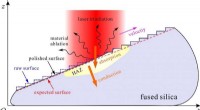
- CO2-laserablatie leidt een nieuw pad naar aangepaste continue gesmolten silica-oppervlakken
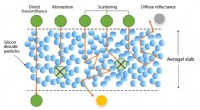
- Aerogels voor zonne-apparaten en ramen
- Video:Is uw katalysator gestolen? Dit is waarom

- Nrl ontvangt patent voor koolstofafvangapparaat - een belangrijke stap in de productie van synthetische brandstof uit zeewater
 Wat zijn de rol van logica voor de wetenschap?
Wat zijn de rol van logica voor de wetenschap?  Wat is de aantrekkingskracht tussen waterstof- en zuurstofatomen in een waterverbinding?
Wat is de aantrekkingskracht tussen waterstof- en zuurstofatomen in een waterverbinding?  Wat is de naam van de microscoop die voornamelijk in de klas wordt gebruikt?
Wat is de naam van de microscoop die voornamelijk in de klas wordt gebruikt?  Een andere naam voor de ionosfeer?
Een andere naam voor de ionosfeer?  Hightech Estland stemt online voor Europees Parlement
Hightech Estland stemt online voor Europees Parlement Kunnen de metalen platen in een elektrochemische cel van hetzelfde metaal worden gemaakt?
Kunnen de metalen platen in een elektrochemische cel van hetzelfde metaal worden gemaakt?  Wat is sterker:nature of nurture?
Wat is sterker:nature of nurture?  Op welke datum de aarde is op de kortste afstand van de zon?
Op welke datum de aarde is op de kortste afstand van de zon?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

