
Wetenschap
Is ferro sulfaat reactiever dan zilvernitraat?
* Activiteitenreeks: Metalen zijn gerangschikt in een serie op basis van hun reactiviteit. Metalen hoger in de serie zijn reactiever dan die lager. IJzer (Fe) is hoger in de activiteitenreeks dan zilver (Ag).
* Verplaatsingsreacties: Een meer reactief metaal kan een minder reactief metaal uit de verbinding verplaatsen in een enkele verplaatsingsreactie. Bijvoorbeeld:
* feso₄ + 2agno₃ → fe (no₃) ₂ + 2ag
In deze reactie verplaatst ijzer (Fe) van ijzersulfaat zilver (Ag) van zilvernitraat, vormt ijzernitraat en metaalzilver. Deze reactie toont de hogere reactiviteit van ijzer.
Aanvullende factoren:
* Oplosbaarheid: Ferrous sulfaat is over het algemeen meer oplosbaar in water dan zilvernitraat. Dit betekent dat het eerder aanwezig is in een vorm die gemakkelijk kan reageren.
* Oxidatietoestand: Het ijzer in ijzersulfaat bevindt zich in de +2 oxidatietoestand, wat een relatief stabiele toestand is, maar het kan verder worden geoxideerd tot +3. Zilver in zilvernitraat bevindt zich al in de hoogste oxidatietoestand (+1), waardoor het minder snel reageert.
Samenvattend: Ferrous sulfaat wordt als reactiever beschouwd dan zilvernitraat vanwege zijn hogere positie in de activiteitenreeks, de neiging om deel te nemen aan verplaatsingsreacties en de in het algemeen grotere oplosbaarheid ervan.
 Noem twee mogelijke fosfaten in de neerslagreactie van koper 2 choloride met natriumfosfaat?
Noem twee mogelijke fosfaten in de neerslagreactie van koper 2 choloride met natriumfosfaat?  Scaffolds bouwen met exotische elementen:onderzoeksteam slaagt erin nieuwe metaal-organische raamwerken te creëren
Scaffolds bouwen met exotische elementen:onderzoeksteam slaagt erin nieuwe metaal-organische raamwerken te creëren Wat is het verschil tussen koolstof 12 en 14?
Wat is het verschil tussen koolstof 12 en 14?  Wat is sterker ofwel palladium op koolstof- of palladiumhydroxide?
Wat is sterker ofwel palladium op koolstof- of palladiumhydroxide?  Neutraal deeltje van een atoom gevonden in de kern?
Neutraal deeltje van een atoom gevonden in de kern?
 Onderzoek naar corridors voor wilde dieren laat zien hoe deze in de loop van de tijd werken
Onderzoek naar corridors voor wilde dieren laat zien hoe deze in de loop van de tijd werken  Klimaatcrisis:hoe maak je ruimte voor 2 miljard bomen op een druk eiland als het VK?
Klimaatcrisis:hoe maak je ruimte voor 2 miljard bomen op een druk eiland als het VK? Hoe een slang te identificeren
Hoe een slang te identificeren  Waarom heeft Wave Rock de vorm van een golf?
Waarom heeft Wave Rock de vorm van een golf? Waarom we gehaktballen groen moeten maken:Nieuw onderzoek onderstreept aanzienlijke voordelen voor het milieu
Waarom we gehaktballen groen moeten maken:Nieuw onderzoek onderstreept aanzienlijke voordelen voor het milieu
Hoofdlijnen
- Welke term beschrijft de theorie dat leven voortkomt uit leven?
- Waar zijn erytrocyten volwassen?
- Biologen ontdekken hoe 'stille' mutaties de eiwitproductie beïnvloeden
- Wat is de functie, heeft het vetweefsel in vetten?
- Welke stoffen heeft het lichaam nodig om cellulaire ademhaling uit te voeren?
- Wat is het structurele en functie -kenmerk van diafyse?
- Unicorn Root herleeft zichzelf na 130 jaar
- Wat voor soort bacteriën voedt zich met dode dingen?
- Sorteer de delen van een nucleïnezuur volgens of elk uitsluitend in DNA -RNA of beide typen zuur is?
- Handdesinfecterend middel opnieuw ontwerpen en doneren 7, 000 gallons om COVID-19 te bestrijden

- Een legering die zijn geheugen behoudt bij hoge temperaturen

- Superspons belooft effectieve giftige opruiming van meren en meer

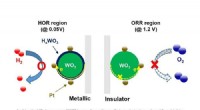
- Wetenschappers lossen een duurzaamheidsprobleem op in brandstofcellen voor waterstofauto's
- Fluorescentiepatronen helpen bij medische diagnostiek

 Wat is de naam van het model dat oorsprong drie basis gesteentetypen illustreert?
Wat is de naam van het model dat oorsprong drie basis gesteentetypen illustreert?  Hoe multitasken werkt
Hoe multitasken werkt  Mysterie opgelost toen Australische duikboot na 103 jaar werd gevonden
Mysterie opgelost toen Australische duikboot na 103 jaar werd gevonden Amazone, Walmart handelt weerhaken op belastingen, loon
Amazone, Walmart handelt weerhaken op belastingen, loon Lage druk, hoge inzet:natuurkundigen boeken grote winst in race voor supergeleiding bij kamertemperatuur
Lage druk, hoge inzet:natuurkundigen boeken grote winst in race voor supergeleiding bij kamertemperatuur Van welk 3 subatomaire deeltje zijn atomen gemaakt?
Van welk 3 subatomaire deeltje zijn atomen gemaakt?  Wat is het verschil tussen poeswilg en treurboom?
Wat is het verschil tussen poeswilg en treurboom?  Wat is de SI -eenheid van kinatische energie?
Wat is de SI -eenheid van kinatische energie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

