
Wetenschap
Hoeveel covalente bindingen kan een atoom van fluor vormen?
Een fluoratoom kan een vormen Covalente binding.
Dit is waarom:
* valentie -elektronen: Fluor heeft 7 valentie -elektronen (elektronen in de buitenste schaal).
* octetregel: Atomen hebben de neiging om elektronen te winnen, verliezen of delen om een stabiele configuratie van 8 valentie -elektronen (de octetregel) te bereiken.
* Bondvorming: Fluor heeft nog een elektron nodig om zijn octet te voltooien. Het bereikt dit door het ene elektron te delen met een ander atoom en een enkele covalente binding te vormen.
 Nieuwe coating brengt lithium-metaalbatterij dichter bij de realiteit
Nieuwe coating brengt lithium-metaalbatterij dichter bij de realiteit Onderzoekers stemmen de snelheid van chiraliteitsschakeling af
Onderzoekers stemmen de snelheid van chiraliteitsschakeling af  Katalysatoren voor isotactische polaire polypropylenen
Katalysatoren voor isotactische polaire polypropylenen Hoe beïnvloeden katalysatoren de botsingstheorie?
Hoe beïnvloeden katalysatoren de botsingstheorie?  Wat betekent het om te zeggen dat een mineraal een bepaalde chemische samenstelling heeft?
Wat betekent het om te zeggen dat een mineraal een bepaalde chemische samenstelling heeft?
 Wat is het manetisme?
Wat is het manetisme?  Eerste detectie van regen boven de oceaan door navigatiesatellieten
Eerste detectie van regen boven de oceaan door navigatiesatellieten Branden in Californië:nieuwe branden terwijl gevaarlijke wind de vlammen aanwakkert
Branden in Californië:nieuwe branden terwijl gevaarlijke wind de vlammen aanwakkert Reactie van wolken op vervuiling opgehelderd met nieuwe klimaatanalyse
Reactie van wolken op vervuiling opgehelderd met nieuwe klimaatanalyse Kan zeegras de verzuring van de oceaan helpen bestrijden?
Kan zeegras de verzuring van de oceaan helpen bestrijden?
Hoofdlijnen
- Wat is een bijzonder kenmerk van de alveolus?
- Wat voor soort wetenschapper die dingen in groepen plaatst?
- Kunnen algen die 'arme leveranciers' zijn, koralen helpen terugkomen na het bleken?
- Wat gebeurt alleen in de Gonads -mitose of meiose?
- Hoe neemt een forel zuurstof in?
- Amerikaans sage hoenbeleid keert terug naar af
- In welk domein gaat een enkel celorganisme met wand maar er geen kern in?
- Hoe snelheid de evolutionaire verandering van de wervelkolom bij zoogdieren beperkt
- Wat leren wetenschappers van ijskernmonsters?
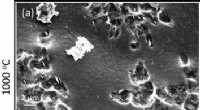
- Onderzoekers fabriceren van polyacrylonitril afgeleide koolstoffilms en vezels bij hoge temperatuur
- Vormverschuivende organische kristallen gebruiken geheugen om plastic elektronica te verbeteren

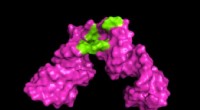
- Onderzoekers ontwikkelen tools om 3D-weergave van grote RNA-moleculen te verscherpen
- Krachten meten van levende cellen en micro-organismen

- Wetenschappers coderen Wizard of Oz in een verdwijnend klein plastic

 Zwaartekracht helpt bij het tonen van een sterke kracht in het proton
Zwaartekracht helpt bij het tonen van een sterke kracht in het proton  Houtspons neemt olie op uit water
Houtspons neemt olie op uit water Kunnen crunch-gesprekken het klimaatverdrag van Parijs tot leven brengen?
Kunnen crunch-gesprekken het klimaatverdrag van Parijs tot leven brengen?  Betere weersvoorspelling door assimilatie van satellietisotoopgegevens
Betere weersvoorspelling door assimilatie van satellietisotoopgegevens Wat is de wetenschappelijke naam voor een verandering in snelheid?
Wat is de wetenschappelijke naam voor een verandering in snelheid?  Supermaan plus zonsverduistering staat gelijk aan zeldzame luchtshow zondagavond (update)
Supermaan plus zonsverduistering staat gelijk aan zeldzame luchtshow zondagavond (update)  Wat is het meest voorkomende type opdringerige rots op aarde?
Wat is het meest voorkomende type opdringerige rots op aarde?  Welk jaar is gelijk aan 84 aardse jaren?
Welk jaar is gelijk aan 84 aardse jaren?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

