
Wetenschap
U krijgt 34,0 g aluminium en 39,0 chloorgas. Als je overtollig had hoeveel mol chloride zou kunnen worden geproduceerd uit aluminium?
1. Schrijf de gebalanceerde chemische vergelijking:
2 Al + 3 Cl₂ → 2 Alcl₃
2. Bereken de mol aluminium:
* Molaire massa van aluminium (AL) =26,98 g/mol
* Mol al =(34,0 g) / (26,98 g / mol) =1,26 mol
3. Bepaal de beperkende reactant:
* Uit de evenwichtige vergelijking reageren 2 mol AL Al met 3 mol CL₂.
* Om volledig te reageren met 1,26 mol AL, zou u (1,26 mol) * (3 mol CL₂ / 2 mol AL) =1,89 mol CL₂ nodig hebben.
* Aangezien je slechts 39,0 g CL₂ hebt, laten we berekenen hoeveel mol dat is:
* Molaire massa chloorgas (CL₂) =70,90 g/mol
* Mol CL₂ =(39,0 g) / (70,90 g / mol) =0,55 mol CL₂
* chloorgas (CL₂) is de beperkende reactant omdat je er minder van hebt dan je nodig hebt om met al het aluminium te reageren.
4. Bereken de mol aluminiumchloride (alcl₃) geproduceerd:
* De gebalanceerde vergelijking laat zien dat 3 mol CL₂ 2 mol ALCL₃ produceert.
* Mol alcl₃ =(0,55 mol Cl₂) * (2 mol ALCL₃ / 3 mol CL₂) =0,37 mol alcl₃
Daarom zou u 0,37 mol aluminiumchloride (ALCL₃) kunnen produceren uit de gegeven hoeveelheden aluminium en chloorgas.
 Effecten van regenwater
Effecten van regenwater Plastic afval bedekt Midden-Amerikaanse rivieren, meren en stranden
Plastic afval bedekt Midden-Amerikaanse rivieren, meren en stranden  Opkomend onkruid blijkt veerkrachtig tegen herbicidenbehandelingen
Opkomend onkruid blijkt veerkrachtig tegen herbicidenbehandelingen  Fruitvliegjes vertonen een verrassende verfijning in het lokaliseren van de voedselbron
Fruitvliegjes vertonen een verrassende verfijning in het lokaliseren van de voedselbron  Wat is het belang van water voor landbouw en volksgezondheid?
Wat is het belang van water voor landbouw en volksgezondheid?
Hoofdlijnen
- Hoe bepalen wetenschappers of ze iets als een organisme moeten beschouwen?
- Wat voor soort wetenschapper bestudeert seks?
- Wat is een organel in het cytoplasma dat energie voor cel levert?
- Snelle weg naar voedselveiligheid:nieuwe test ontdekt ziekteverwekker in zeevruchten in 30 minuten
- Witte bloedcellen vormen de basis van welk systeem in lichaam?
- Wie is Master of Biology?
- Het experiment van Popper werd opnieuw gerealiseerd, maar wat betekent het?
- Hoe beslissen wetenschappers welke informatie te verzamelen?
- Hoeveel elementen is een levend organisme dat bestaat?
- Stralingsweerstand testen zonder een kernreactor te gebruiken

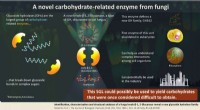
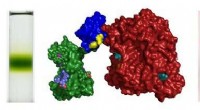
- Nieuwe familie in de buurt:een nieuwe groep glycosidische enzymen
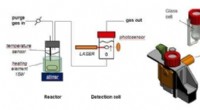
- Nieuw eenvoudig apparaat verbetert de analyse van de reactiekinetiek aanzienlijk
- Nieuwe methode om het comfort van slim en functioneel textiel te evalueren

- Team ontwikkelt fotosynthetische eiwitten voor uitgebreide omzetting van zonne-energie
 Wat is meer donker dan de nacht?
Wat is meer donker dan de nacht?  Is het mogelijk om één kracht te hebben?
Is het mogelijk om één kracht te hebben?  Waarom honden er niet om geven verzorgd te worden (en de liefde voor honden hun snorharen afknipt)
Waarom honden er niet om geven verzorgd te worden (en de liefde voor honden hun snorharen afknipt)  3D-simulatie laat zien hoe de vorm van complexe organen evolueert door natuurlijke selectie
3D-simulatie laat zien hoe de vorm van complexe organen evolueert door natuurlijke selectie  Is energie verloren tijdens de overdracht van niveaus?
Is energie verloren tijdens de overdracht van niveaus?  Wat vertelt de rotscycli over het aardproces?
Wat vertelt de rotscycli over het aardproces?  De fysica van lopen verduidelijken:voor wezens met meerdere poten lijkt het veel op glijden
De fysica van lopen verduidelijken:voor wezens met meerdere poten lijkt het veel op glijden Landbouw en chemische oorlogsvoering:een dag uit het leven van een mier?
Landbouw en chemische oorlogsvoering:een dag uit het leven van een mier?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

