
Wetenschap
Wat is het aantal atomen in PB van 103,6 gram?
Hier leest u hoe u het aantal atomen in 103,6 gram lood (PB) kunt berekenen:
1. Vind de molaire leadmassa:
* De molaire kabelmassa (PB) is 207,2 g/mol (u kunt dit vinden op het periodieke tabel).
2. Bereken het aantal mol lood:
* Mol =massa / molaire massa
* Mol =103,6 g / 207,2 g / mol
* Mol =0,5 mol
3. Gebruik het nummer van Avogadro om het aantal atomen te vinden:
* Het nummer van Avogadro is 6.022 x 10^23 atomen/mol.
* Aantal atomen =mollen * Avogadro's nummer
* Aantal atomen =0,5 mol * 6.022 x 10^23 atomen/mol
* Aantal atomen =3.011 x 10^23 Atomen
Daarom zijn er ongeveer 3,011 x 10^23 atomen in 103,6 gram lood.
 Wat voor soort binding zal het gevolg zijn wanneer twee identieke niet -metalen atomen combineren?
Wat voor soort binding zal het gevolg zijn wanneer twee identieke niet -metalen atomen combineren?  Wat is een proces dat vloeibare oliën stolt en stabiliseert?
Wat is een proces dat vloeibare oliën stolt en stabiliseert?  Onderzoekers ontwikkelen een unieke methode om 3D poreuze structuren te fabriceren
Onderzoekers ontwikkelen een unieke methode om 3D poreuze structuren te fabriceren Kan waterstof een vaste stof worden?
Kan waterstof een vaste stof worden?  Wat is de uitgebalanceerde vergelijking van calciumcarbonaat dat reageert met fosforzuur?
Wat is de uitgebalanceerde vergelijking van calciumcarbonaat dat reageert met fosforzuur?
 Plastics zullen kolen overtreffen in Amerikaanse CO2-emissies, studieshows
Plastics zullen kolen overtreffen in Amerikaanse CO2-emissies, studieshows Californië geteisterd door bosbranden, warmte, ongezonde rokerige lucht
Californië geteisterd door bosbranden, warmte, ongezonde rokerige lucht Slimme containers om mensen te belonen voor goed recyclen
Slimme containers om mensen te belonen voor goed recyclen Bosbranden verschroeien huizen van de rijken en beroemdheden in Los Angeles
Bosbranden verschroeien huizen van de rijken en beroemdheden in Los Angeles De lange schaduw van koloniale bosbouw vormt een bedreiging voor savannes en graslanden
De lange schaduw van koloniale bosbouw vormt een bedreiging voor savannes en graslanden
Hoofdlijnen
- Welk percentage van een plantencel is water?
- Welk celorganel regelt de synthese van enzymen?
- Nieuw onderzoek met video laat zien hoe vrouwelijke kikkers zich verdedigen tegen ongewenste paring
- Welke kenmerken die mensen bezitten die anders zijn dan andere organismen?
- Interne membranen spelen een belangrijke rol bij de productie en verwerking van eiwitten, behalve dat ze dat niet doen?
- Organismen gemaakt van prokaryotische cellen worden gevonden in welk koninkrijk?
- Dankzij een krachtige nieuwe techniek kunnen wetenschappers bestuderen hoe eiwitten in cellen van vorm veranderen
- Wat is het belangrijkste punt van evolutie in verwijzing naar ontwikkeling?
- Hoe mannen voortdurend sperma produceren – en hoe die ontdekking onvruchtbaarheid kan helpen behandelen
- Onderzoek onthult structuur van humane endogene reverse transcriptase
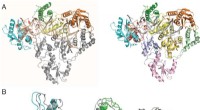
- Het beste van twee werelden:hoge entropie ontmoet lage dimensies, opent oneindige mogelijkheden

- Op de natuur geïnspireerde antibacteriële metalen

- Een nieuw proces voor volledig gebruik van zachthoutschors

- Bibliotheek met spinnenzijde kan geheimen bevatten voor nieuwe materialen

 Nieuwe studie traceert vulkanische getijden van Ios
Nieuwe studie traceert vulkanische getijden van Ios 10 geweldige dingen die de hersenen van mensen hebben gedaan
10 geweldige dingen die de hersenen van mensen hebben gedaan  Hoe melkveehouders zich kunnen aanpassen aan de klimaatverandering
Hoe melkveehouders zich kunnen aanpassen aan de klimaatverandering  Wat is een trans-soort sprong?
Wat is een trans-soort sprong?  Emotionele AI en generatie Z:de houding ten opzichte van nieuwe technologie en haar zorgen
Emotionele AI en generatie Z:de houding ten opzichte van nieuwe technologie en haar zorgen Wat is 0,9 Celsius -graad gelijk aan Fahrenheit?
Wat is 0,9 Celsius -graad gelijk aan Fahrenheit?  Natuurkundigen ontwikkelen zeer robuuste tijdkristallen
Natuurkundigen ontwikkelen zeer robuuste tijdkristallen  Hoe zou u energie definiëren?
Hoe zou u energie definiëren?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

