
Wetenschap
Waarom leidt vloeibare KCL elektriciteit?
* ionische verbinding: KCL (kaliumchloride) is een ionische verbinding, wat betekent dat deze wordt gevormd door de elektrostatische aantrekkingskracht tussen positief geladen kaliumionen (k+) en negatief geladen chloride-ionen (Cl-).
* vaste toestand: In zijn vaste toestand worden de ionen gehouden in een rigide, kristallijne roosterstructuur. Dit voorkomt dat de ionen vrijuit bewegen, dus solide KCL is een slechte geleider van elektriciteit.
* vloeibare status: Wanneer KCL wordt gesmolten, worden de sterke elektrostatische krachten die de ionen op hun plaats houden, overwonnen. Hierdoor kunnen de ionen loskomen van het rooster en onafhankelijk bewegen.
* Laad dragers: De beweging van deze vrij bewegende ionen (zowel positief als negatief) draagt elektrische stroom. De positief geladen kaliumionen bewegen naar de negatieve elektrode, terwijl de negatief geladen chloride -ionen naar de positieve elektrode bewegen.
In wezen leidt vloeibare KCL elektriciteit omdat het vrije verkeer van zijn ionen de ladingsstroom mogelijk maakt.
 De bescherming en het behoud van het milieu door het beheren van natuurlijke hulpbronnen wordt genoemd?
De bescherming en het behoud van het milieu door het beheren van natuurlijke hulpbronnen wordt genoemd?  Bewijs voor aanhoudende afhankelijkheid van bossen door inheemse volkeren in het historische Sri Lanka
Bewijs voor aanhoudende afhankelijkheid van bossen door inheemse volkeren in het historische Sri Lanka Bomcyclonen - de intense winterstormen die de VS (en ook Australië) troffen
Bomcyclonen - de intense winterstormen die de VS (en ook Australië) troffen Wat zijn de oorzaken van gevaarlijk afval?
Wat zijn de oorzaken van gevaarlijk afval?  Arctische verandering heeft wijdverbreide gevolgen
Arctische verandering heeft wijdverbreide gevolgen
Hoofdlijnen
- Hoe in een laboratorium gekweekte huid werkt
- Waar wordt protease in uw lichaam gevonden?
- De manier waarop een cyanobacterie omgaat met ijzerschaarste maakt hem tot het meest succesvolle fotosynthetische organisme op aarde
- Een 3D-poster maken van de celcyclus
- Welk type plant wordt gebruikt om tabak te maken?
- Hoe planten 'slechte' moleculen benutten voor goede doeleinden
- Geleidelijke opwarming van de aarde culmineerde aan het einde van het Perm in een gigantische uitstervingsgebeurtenis, studievondsten
- Welk type cel vernietigt lichaamscellen die zijn geïnfecteerd met microben?
- Verschillen en overeenkomsten tussen Unicellular & Cellular
- Duurzame houtsponzen fungeren als groene sensoren voor mechanische belasting

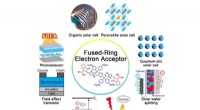
- Vooruitgang in gefuseerde-ringelektronenacceptoren
- Onderzoekers benutten de kracht van carbenen om drugs gemakkelijker en veiliger te fabriceren
- Wetenschappers produceren eerste open source all-atom-modellen van COVID-19 spike-eiwit

- Maskers slimmer en veiliger maken tegen COVID-19
 Wat is het vangen van zonnestraling?
Wat is het vangen van zonnestraling?  Onderzoek helpt terrein te ruimen om land schoon te maken
Onderzoek helpt terrein te ruimen om land schoon te maken Polarisatie van broommolecuul in vanadiumoxideclusterholte en nieuwe bromering van alkaan
Polarisatie van broommolecuul in vanadiumoxideclusterholte en nieuwe bromering van alkaan Wat is het land van Seven Hills?
Wat is het land van Seven Hills?  Het mengen van meren – de macht van het micro-organisme
Het mengen van meren – de macht van het micro-organisme Kan COVID-19 inspireren tot een nieuwe manier om Afrikaanse steden te plannen?
Kan COVID-19 inspireren tot een nieuwe manier om Afrikaanse steden te plannen? Welk type energietransformatie is het wanneer de elektrische broodrooster op het stopcontact werd aangesloten en vroeger diner maakte?
Welk type energietransformatie is het wanneer de elektrische broodrooster op het stopcontact werd aangesloten en vroeger diner maakte?  Hoe communicatiekanalen te berekenen
Hoe communicatiekanalen te berekenen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

