
Wetenschap
Wanneer 0,422 g van een fosfor wordt verbrand. 0,967 wit oxide verkregen wat de empirische formule en ook evenwichtige vergelijking voor reactie O2 van EF?
1. Bepaal de massa zuurstof:
* Massa van zuurstof =Massa van oxide - Massa van fosfor
* Massa van zuurstof =0,967 g - 0,422 g =0,545 g
2. Converteer massa's naar mollen:
* Mol fosfor =massa van fosfor / molaire massa van fosfor
* Mol fosfor =0,422 g / 30,97 g / mol =0,0136 mol
* Mol zuurstof =massa zuurstof / molaire zuurstofmassa
* Mol zuurstof =0,545 g / 16,00 g / mol =0,0341 mol
3. Vind de molverhouding:
* Verdeel het aantal mol van elk element door het kleinste aantal mol:
* Fosfor:0,0136 mol / 0,0136 mol =1
* Zuurstof:0,0341 mol / 0,0136 mol =2,5
4. Converteer naar hele getallen:
* Aangezien we een verhouding van 1:2.5 hebben, vermenigvuldig beide zijden met 2 om hele getallen te krijgen:
* Fosfor:1 x 2 =2
* Zuurstof:2,5 x 2 =5
5. Empirische formule:
* De empirische formule van het fosforoxide is p₂o₅ .
6. Evenwichtige chemische vergelijking:
* De evenwichtige chemische vergelijking voor de reactie van fosfor met zuurstof is:
4 P + 5 O₂ → 2 P₂o₅
Verklaring:
* De empirische formule vertegenwoordigt de eenvoudigste verhouding van het hele nummer van atomen in een verbinding.
* De evenwichtige chemische vergelijking zorgt ervoor dat het aantal atomen van elk element hetzelfde is aan beide zijden van de vergelijking, volgens de wet van behoud van massa.
Hoofdlijnen
- Hoeveel delen is het menselijk lichaam verdeeld?
- Wat betekent biotische factor?
- Wat voor soort parasiet zijn schurft?
- Waarom is een academisch woord?
- Wat experimenteerde Frederick met muizen?
- Vijf minuten wandelen is de beste manier om huilende baby's te troosten, zegt onderzoek
- Wat zijn de vier basiseenheden afgeleid van voedsel?
- Wat is de wetenschappelijke naam van een herbivoor en een carnivoor?
- Onderzoek geeft inzicht in hoe maïs hormonen aanmaakt
- Een nieuwe manier om pompoenkruiden te maken, verdovende middelen, cosmetica

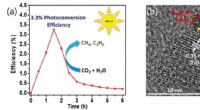
- Een-twee-stempel katalysatoren die koolstofdioxide opvangen voor schonere brandstoffen
- Onzichtbaar, rekbare circuits om de volgende generatie technologie vorm te geven

- Voorkomen van infectie, genezing vergemakkelijken:nieuwe biomaterialen van spinnenzijde

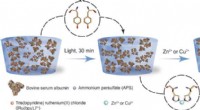
- Kation-geïnduceerde vormprogrammering en morphing in op eiwit gebaseerde hydrogels
 Hoe en zonnebrand werken
Hoe en zonnebrand werken  Als K en L -shell van een atoom vol zijn, wat zijn dan de nummerelektronen in Atom?
Als K en L -shell van een atoom vol zijn, wat zijn dan de nummerelektronen in Atom?  Welke energie van de interne hitte van de aarde?
Welke energie van de interne hitte van de aarde?  Komt naar een monitor bij u in de buurt:Een storingsvrij, molecuul-dikke film
Komt naar een monitor bij u in de buurt:Een storingsvrij, molecuul-dikke film Hoeveel natriumatrium zal combineren met één atoomchloor?
Hoeveel natriumatrium zal combineren met één atoomchloor?  Wat is dynamiet en hoe werkt het?
Wat is dynamiet en hoe werkt het?  Wat is het verschil tussen draagvermogen en biotisch potentieel?
Wat is het verschil tussen draagvermogen en biotisch potentieel?  Het Canadese bosbrandenseizoen begint
Het Canadese bosbrandenseizoen begint
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


