
Wetenschap
Wat is moleculaire geometrie van CL2?
Dit is waarom:
* Lewis -structuur: Chloor heeft 7 valentie -elektronen. In CL₂ deelt elk chlooratoom het ene elektron met het andere, wat een enkele covalente binding vormt. Dit resulteert in beide chlooratomen met een compleet octet.
* vSEPR -theorie: De theorie van de valentieschaal elektronenparen (VSEPR) voorspelt de vorm van moleculen op basis van de afstoting tussen elektronenparen rond het centrale atoom. In CL₂ zijn er geen eenzame paren elektronen op beide chlooratoom, alleen het gedeelde paar in de binding.
* lineaire geometrie: Met twee atomen en geen eenzame paren is de enige mogelijke opstelling een rechte lijn, wat resulteert in een lineaire moleculaire geometrie.
 Wat is de samengestelde formule voor zilverhydride?
Wat is de samengestelde formule voor zilverhydride?  Wat voor soort chemische reactie komt het meest voor op de actieve site?
Wat voor soort chemische reactie komt het meest voor op de actieve site?  Toont 3 octeen cis trans -isomerisme?
Toont 3 octeen cis trans -isomerisme?  Hoe AI en diepere wortels de bodem kunnen helpen meer koolstof op te slaan
Hoe AI en diepere wortels de bodem kunnen helpen meer koolstof op te slaan  Medicijnen ontwerpen die gericht zijn op een ander deel van de levenscode
Medicijnen ontwerpen die gericht zijn op een ander deel van de levenscode
 Rusland sluit zich aan bij klimaatakkoord Parijs
Rusland sluit zich aan bij klimaatakkoord Parijs Wie heeft Jamestown geleerd om planten te laten groeien?
Wie heeft Jamestown geleerd om planten te laten groeien?  NASA jaarlijkse Arctische ijsonderzoek uitgebreid bereik dit jaar
NASA jaarlijkse Arctische ijsonderzoek uitgebreid bereik dit jaar Waarom was frenologie zo populair in de Victoriaanse tijd?
Waarom was frenologie zo populair in de Victoriaanse tijd?  NASA-luchtlandingsmissie keert terug naar Afrika om rook te bestuderen, wolken
NASA-luchtlandingsmissie keert terug naar Afrika om rook te bestuderen, wolken
Hoofdlijnen
- Wat zijn fotoblastische cellen?
- Artificiële intelligentie gebruiken om tuberculosebehandelingen te verbeteren
- Welke receptorcellen zijn er in slijm membraan?
- Hoe medicijnresistente ziekteverwekkerstammen elkaar ontmoeten en evolueren op bloembollen
- Wat is er met gapen?
- DNA-ontdekking kan licht werpen op zeldzame kinderziekte
- Een model waarmee planten hun fotosynthetische stofwisseling aanpassen aan de lichtintensiteit
- Een driedimensionaal tandmodel maken voor een schoolproject
- Wat is heemopoiesis?
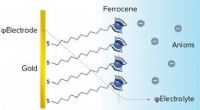
- Gecombineerde aanpak om grensvlakelektrochemie in meer detail te onderzoeken
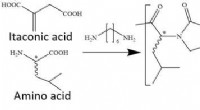
- Pepsine-afbreekbare plastics van bio-nylons van itacon en aminozuren
- De chemie van de aarde modelleren:het onzichtbare zichtbaar maken

- Mangaan drukt zijn stempel op de synthese van geneesmiddelen

- Beheers de chaos om keramiek met hoge entropie te maken

 Welk type energie gebruikt een match?
Welk type energie gebruikt een match?  Gedragen thorium warmte en elektriciteit?
Gedragen thorium warmte en elektriciteit?  H3o Plus is een polair of niet -polair molecuul?
H3o Plus is een polair of niet -polair molecuul?  Hoe vind je de Melkweg in de nachtelijke hemel?
Hoe vind je de Melkweg in de nachtelijke hemel?  Wat is de uiteindelijke snelheid van een vrij vallend object?
Wat is de uiteindelijke snelheid van een vrij vallend object?  Vijf van de belangrijkste ontdekkingen aan boord van NASA's Curiosity-rover op Mars
Vijf van de belangrijkste ontdekkingen aan boord van NASA's Curiosity-rover op Mars Hoe chloor next-gen zonnecellen stabiliseert op atomaire schaal
Hoe chloor next-gen zonnecellen stabiliseert op atomaire schaal Wat is galio?
Wat is galio?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

