
Wetenschap
Welke verhouding kunt u bepalen met behulp van de coëfficiënt in een chemische formule?
Hier is hoe het werkt:
* coëfficiënten: De getallen voor elke chemische formule in een gebalanceerde vergelijking worden coëfficiënten genoemd. Ze vertegenwoordigen het relatieve aantal mol van elke substantie die bij de reactie betrokken is.
* molverhouding: De coëfficiënten bieden een directe vergelijking van het aantal mol mol van elke reactant en product.
Voorbeeld:
Overweeg de evenwichtige vergelijking voor de verbranding van methaan:
Ch₄ + 2o₂ → co₂ + 2h₂o
* Coëfficiënt van Ch₄: 1
* Coëfficiënt van O₂: 2
* coëfficiënt van co₂: 1
* Coëfficiënt van H₂o: 2
Dit vertelt ons dat:
* 1 mol methaan (ch₄) reageert met 2 mol zuurstof (o₂)
* 1 mol methaan (ch₄) produceert 1 mol kooldioxide (CO₂) en 2 mol water (H₂o)
Sleutelpunt: De molverhouding is cruciaal voor het begrijpen van de stoichiometrie van chemische reacties en voor het uitvoeren van berekeningen met hoeveelheden reactanten en producten.
 Wat bestaat molecuul uit één koolstofatoom en twee zuurstofatomen correct geschreven als?
Wat bestaat molecuul uit één koolstofatoom en twee zuurstofatomen correct geschreven als?  Methanolbiotransformatie maakt efficiënte productie van vetzuren uit gist mogelijk
Methanolbiotransformatie maakt efficiënte productie van vetzuren uit gist mogelijk Waarom heeft water mei chemicaliën erin opgelost?
Waarom heeft water mei chemicaliën erin opgelost?  Wat zijn de 2 producten gevormd in een neutralisatiereactie?
Wat zijn de 2 producten gevormd in een neutralisatiereactie?  Chemie Onderwerpen voor Cursus Presentaties
Chemie Onderwerpen voor Cursus Presentaties
 Kleine zandkorrels veroorzaken enorme gletsjergolven
Kleine zandkorrels veroorzaken enorme gletsjergolven Wat de Amerikaanse defensie-industrie ons kan vertellen over de strijd tegen klimaatverandering
Wat de Amerikaanse defensie-industrie ons kan vertellen over de strijd tegen klimaatverandering In welke richting zijn de grote meren van ons?
In welke richting zijn de grote meren van ons?  NASA meet de sterkte van tropische stormdelta's in infrarood
NASA meet de sterkte van tropische stormdelta's in infrarood Onderzoek naar materialen in diepe aarde om het evolutionaire verhaal van de aarde te ontcijferen
Onderzoek naar materialen in diepe aarde om het evolutionaire verhaal van de aarde te ontcijferen
Hoofdlijnen
- Wie was een Italiaanse Abbott en bioloog wiens wetenschappelijke onderzoeken volgden op experimenten met spontane generatie?
- Virusgenomen helpen verklaren waarom een belangrijke veeziekte opnieuw de kop opsteekt in Europa
- Wat organiseert het genoom in de kern?
- Wat heeft Howard Florey bijgedragen aan de wetenschap?
- Waarom is een ziekte eerder geneigd om elk van de groepsplanten die door de weefselkweek zijn geproduceerd dan zaad te doden?
- Waarom zijn er minder organismen op de hogere trofische niveaus dan op de lagere niveaus?
- Wat is mutatie en hoe kan een organisme beïnvloeden?
- The Anatomy of the Hydra
- Hoe zijn schimmels en planten vergelijkbaar?
- Lasers gebruiken om moleculaire mysteries in onze atmosfeer te visualiseren

- Onderzoekers brengen kristallen in kaart om behandelingen voor beroerte te bevorderen, suikerziekte, Dementie
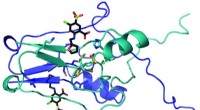
- Prullenbak om te koesteren:wetenschappers zetten gemeentelijk afval om in voorlopers van biobrandstoffen

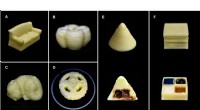
- Onderzoekers ontwikkelen eenvoudige methode om melkproducten in 3D te printen
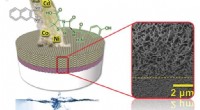
- Nieuw, op waterbasis, recyclebare membraanfilters alle soorten nanodeeltjes
 Wat eet de witte schildpadbloem?
Wat eet de witte schildpadbloem?  Welk type energie wordt geproduceerd in een blikopener produceren?
Welk type energie wordt geproduceerd in een blikopener produceren?  Hoe kunt u energie krijgen van een waterwiel?
Hoe kunt u energie krijgen van een waterwiel?  Waarom wordt siliconenolie gebruikt in smeltpuntapparatuur?
Waarom wordt siliconenolie gebruikt in smeltpuntapparatuur?  Wat zijn de belangrijkste kenmerken en voordelen van Astro FI 102mm Maksutov-CasSegrain-telescoop?
Wat zijn de belangrijkste kenmerken en voordelen van Astro FI 102mm Maksutov-CasSegrain-telescoop?  Ontwikkeling bedreigt tropische bossen, onderzoekers zeggen:
Ontwikkeling bedreigt tropische bossen, onderzoekers zeggen: De netto kracht f versnelt een massa M met een versnelling Wat resulteert als 2f op 4m werkt?
De netto kracht f versnelt een massa M met een versnelling Wat resulteert als 2f op 4m werkt?  Amerikaanse sondeercertificering van Boeing 737 MAX
Amerikaanse sondeercertificering van Boeing 737 MAX
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

