
Wetenschap
Wat is de formule voor ontleding van zinknitraat in oxide stikstofdioxide zuurstof?
2 Zn (No₃) ₂ (s) → 2 ZnO (s) + 4 no₂ (g) + o₂ (g)
Hier is een uitsplitsing van de reactie:
* Zn (no₃) ₂ (s): Zinknitraat, in zijn vaste toestand (s)
* Zno (s): Zinkoxide, in zijn vaste toestand (en)
* no₂ (g): Stikstofdioxide, in zijn gasvormige toestand (g)
* o₂ (g): Zuurstofgas, in zijn gasvormige toestand (g)
Verklaring:
Dit is een ontledingsreactie, waarbij een reactant uiteenvalt in meerdere producten. In dit geval zorgt de warmte ervoor dat de nitraationen (NO₃⁻) ontbinden, waardoor stikstofdioxide (NO₂) en zuurstofgas (O₂) wordt vrijgeeft. De zinkkationen (Zn²⁺) combineren vervolgens met de zuurstofionen om zinkoxide (ZnO) te vormen.
Sleutelpunten:
* Deze reactie vereist warmte om de ontleding te initiëren.
* De coëfficiënten in de gebalanceerde vergelijking (2, 2, 4, 1) zorgen ervoor dat het aantal atomen van elk element hetzelfde is aan beide zijden van de vergelijking.
* De producten zijn een mengsel van vaste, vloeistof en gasvormige fasen.
 Hoe slaan schorren koolstof op?
Hoe slaan schorren koolstof op?  Apparaten die worden gebruikt om verontreinigende stoffen uit rookstapels te verwijderen
Apparaten die worden gebruikt om verontreinigende stoffen uit rookstapels te verwijderen E-mails herhalen de banden van EPA-leiders met belangen in fossiele brandstoffen
E-mails herhalen de banden van EPA-leiders met belangen in fossiele brandstoffen ExxonMobil vindt grootste gasreserve van Cyprus tot nu toe
ExxonMobil vindt grootste gasreserve van Cyprus tot nu toe Wanneer rotsen veranderen in de rotscyclus, zien we een voorbeeld van conservering, wat?
Wanneer rotsen veranderen in de rotscyclus, zien we een voorbeeld van conservering, wat?
Hoofdlijnen
- Nadat een regenboat is geworden dat regenwormen op het trottoir of de weg kunnen kruipen, hoe zou de theorie van spontane generatie orginwormen verklaren?
- Waarom worden enzymen beschouwd als Songior in vergelijking met andere gekatalyseerde?
- Waarom hebben jullie botcellen en rood bloed minder mitochondriën?
- Het voortbestaan van de bedreigde monarchvlinder hangt af van instandhouding buiten de grenzen
- Welk bewijs is aanwezig Prokaryoten bestonden vóór eukaryoten?
- Geleidelijke opwarming van de aarde culmineerde aan het einde van het Perm in een gigantische uitstervingsgebeurtenis, studievondsten
- Welk type cellen zou meer mitochondriën hebben en waarom?
- Hoe kan ik honing uit een wilde bijenkorf extraheren?
- Wat is een cel die geen kern heeft?
- Nieuwe hydrogels verdorren terwijl stamcellen bloeien voor weefselherstel

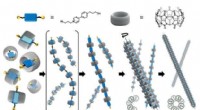
- Zelf-geassembleerde kunstmatige microtubuli zoals LEGO-bouwstenen
- Happy hour voor tijdopgeloste kristallografie
- Vervaardiging van metaal-organische framegebaseerde composieten voor efficiëntie

- Oplossingsverwerkte OLED's maken de weg vrij voor toekomstige verlichtingstoepassingen

 Emissies veroorzaken vertraging in regenval
Emissies veroorzaken vertraging in regenval Wat zijn de drie delen van de kinetische theorie?
Wat zijn de drie delen van de kinetische theorie?  Breuken met decimalen vereenvoudigen
Breuken met decimalen vereenvoudigen  NASA bespioneert formatie tropische cycloon 08Ps
NASA bespioneert formatie tropische cycloon 08Ps Een eendwaddles 2,5 m oost en 6.0 North Wat zijn de verplaatsingsrichting met betrekking tot zijn oorspronkelijke positie?
Een eendwaddles 2,5 m oost en 6.0 North Wat zijn de verplaatsingsrichting met betrekking tot zijn oorspronkelijke positie?  Hoe brandweerwagens werken
Hoe brandweerwagens werken  Experimenteel een toffoli-poort gedemonstreerd in een halfgeleidersysteem met drie qubits
Experimenteel een toffoli-poort gedemonstreerd in een halfgeleidersysteem met drie qubits Wat is de procedure op het laboratoriumapparaat van natuurkunde?
Wat is de procedure op het laboratoriumapparaat van natuurkunde?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

