
Wetenschap
Een oplossing van ammoniak wordt toegevoegd aan een ijzerchloride?
De reactie:
* ferrische ionen (Fe³⁺) reageren met ammoniak (NH₃) om een complexe ion te vormen genaamd hexaammineiron (iii) ion [fe (nH₃) ₆] ³⁺:
Fe³⁺ (aq) + 6nh₃ (aq) → [fe (nH₃) ₆] ³⁺ (aq)
* De [Fe (NH₃) ₆] ³⁺ ion wordt vervolgens gehydrolyseerd in water, wat resulteert in de afgifte van H⁺ -ionen en vorming van een hydroxide -neerslag (Fe (OH) ₃):
[Fe (NH₃) ₆] ³⁺ (aq) + 3h₂o (l) → fe (oh) ₃ (s) + 6nh₄⁺ (aq)
Het resultaat:
* Het waargenomen roodbruine neerslag is ferrische hydroxide (Fe (OH) ₃) .
* De oplossing bevat ook ammoniumionen (NH₄⁺).
Aanvullende opmerkingen:
* Het aantal toegevoegde ammoniak bepaalt de uitkomst.
* Als ammoniak overtollig wordt toegevoegd, kan het neerslag oplossen om een kleurloze oplossing te vormen die de [Fe (NH₃) ₆] ³⁺ complexion bevat.
* De reactie is een voorbeeld van een complexatiereactie, waarbij een metaalion een complex vormt met liganden (in dit geval ammoniakmoleculen).
* De vorming van het neerslag is een omkeerbare reactie. Het toevoegen van zuur kan het neerslag opnieuw oplossen door het evenwicht te verplaatsen naar de vorming van [Fe (NH₃) ₆] ³⁺.
Deze reactie is een veel voorkomende laboratoriumtest voor de aanwezigheid van ijzerionen.
Hoofdlijnen
- Minimale zuurstofconcentratie voor menselijke ademhaling
- Live 3D-beeldvorming benadrukt cellulaire activiteit tijdens embryonale hartontwikkeling
- Wat zijn de sterke punten van de biogenesetheorie?
- Geheimen van sargassum:wetenschappers vergroten de kennis over zeewier dat chaos veroorzaakt in het Caribisch gebied en West-Afrika
- Apen vertonen dramatisch verschillende vroege immuunreacties vergeleken met apen
- Wat zijn enkele voorbeelden van wetenschappelijke teksten?
- Hoe dieren hun juiste maat bereiken
- Wetenschappers introduceren DIProT:een interactieve deep learning-toolkit voor efficiënt eiwitontwerp
- Hoe worden levende organismen momenteel gecategoriseerd?
- Het degradatiegedrag van geavanceerde medische apparaten voorspellen

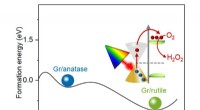
- Verbetering van de productie van waterstofperoxide door duurzame fotokatalyse
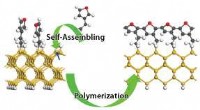
- Nieuwe route naar moleculaire draden geschikt voor gebruik in miniatuurelektronica
- Ontdekking van hoe mensen de geur van de dood ervaren, kan levens redden

- Nieuwe studie helpt bij het karakteriseren van de fusie van metalen

 Wat is een stof die natriumlaurylsulfaat bevat?
Wat is een stof die natriumlaurylsulfaat bevat?  Associatieve & commutatieve eigenschappen van vermenigvuldiging
Associatieve & commutatieve eigenschappen van vermenigvuldiging  Hoeveel sterren van sterren?
Hoeveel sterren van sterren?  Wordt natriumhydroxide verkregen uit rotszout?
Wordt natriumhydroxide verkregen uit rotszout?  Welke energietransformaties komen voor wanneer u een helling op een helling hebt geklaard?
Welke energietransformaties komen voor wanneer u een helling op een helling hebt geklaard?  Op welke elementen zijn macromoleculen gebaseerd?
Op welke elementen zijn macromoleculen gebaseerd?  Welke enzymen zijn verantwoordelijk voor de afbraak van zetmeel?
Welke enzymen zijn verantwoordelijk voor de afbraak van zetmeel?  In Rutherfords Gold Foil Experiment Sommige van de gericht op atomen teruggestuurd om te suggereren dat een vaste massa centrumatoom was?
In Rutherfords Gold Foil Experiment Sommige van de gericht op atomen teruggestuurd om te suggereren dat een vaste massa centrumatoom was?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


