
Wetenschap
In Rutherfords Gold Foil Experiment Sommige van de gericht op atomen teruggestuurd om te suggereren dat een vaste massa centrumatoom was?
* Het experiment: Rutherford vuurde alfa -deeltjes (positief geladen deeltjes) op een dunne vel goudfolie. Hij verwachtte dat de deeltjes dwars door zouden gaan, of hoogstens enigszins afgebogen zouden worden.
* onverwachte resultaten: Tot zijn verbazing stuiterde een klein percentage van de alfa -deeltjes onder grote hoeken terug, sommige zelfs bijna meteen terug naar de bron!
* De interpretatie: Dit onverwachte verstrooiingspatroon bracht Rutherford ertoe het volgende voor te stellen:
* Een dichte, positief geladen kern: Hij concludeerde dat de gouden atomen een klein, dicht, positief geladen centrum moeten bevatten, dat hij de kern noemde. Deze kern was verantwoordelijk voor het afstoten van de positief geladen alfa -deeltjes.
* Het atoom is meestal lege ruimte: Omdat de meeste alfa -deeltjes dwars door de folie gingen, besefte Rutherford dat het grootste deel van het volume van het atoom lege ruimte was. Men dacht dat de elektronen in een wolkachtige structuur om deze kern draaien.
Kortom, de alfa -deeltjes die terug stuiteren, suggereerden direct de aanwezigheid van een vaste, dichte massa (de kern) in het midden van elk goudatoom. Deze ontdekking bracht een revolutie teweeg in ons begrip van de atomaire structuur en maakte de weg vrij voor toekomstige vooruitgang in de nucleaire fysica.
 Hoe het meten van de massa van een vaste stof anders is dan de vloeistof die uitlegt?
Hoe het meten van de massa van een vaste stof anders is dan de vloeistof die uitlegt?  Hoeveel mol CO2 worden geproduceerd uit de reactie drie acetyleen met overtollige zuurstof?
Hoeveel mol CO2 worden geproduceerd uit de reactie drie acetyleen met overtollige zuurstof?  Welke atomen worden gevonden dat ik eiwitten ben?
Welke atomen worden gevonden dat ik eiwitten ben?  Hebben enzymen in de dunne darm een zure omgevingsvolgorde nodig om te werken?
Hebben enzymen in de dunne darm een zure omgevingsvolgorde nodig om te werken?  "What is an Arrhenius Acid?
"What is an Arrhenius Acid?
Hoofdlijnen
- Ontdekken hoe bedreigde schubdieren, of 'geschubde miereneters', voedsel verteren
- Wie was een van de mannen die de basisceltheorie vormden?
- Als u een adenine vindt op een sporten DNA met welke basis wordt deze verbonden?
- Wat is de plaats van eiwitsynthese in cel -samengesteld rRNA en eiwit?
- Wat houdt cellen in vorm? Nieuw onderzoek wijst op twee soorten bewegingen
- UITLEGGER:Wat is een derecho?
- Onderzoeker zegt:No-till-praktijken laten uitgebreide voordelen zien voor tarwe en veevoer
- Was de grote omvang van de sauropode dinosaurussen te danken aan plantaardig voedsel? Wetenschappers beweren dat het oude idee nog steeds benen heeft
- Wat is de groep organismen die voedsel maken voor een ecosysteem?
- Atoms kunnen een deuntje neuriën uit een grootse kosmische symfonie

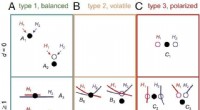
- Bayesiaanse modelselectie vertoont extreem gepolariseerd gedrag wanneer de modellen fout zijn
- Studie suggereert twee nieuwe methoden om naar donkere materie te zoeken door kleine verstoringen in fundamentele constanten te meten

- Halfgeleiderapparaten met een brede bandgap op basis van siliciumcarbide kunnen een revolutie teweegbrengen in de elektronica

- Ultradunne film creëert levendige 3D-beelden met een groot gezichtsveld

 Wie is verantwoordelijk als klimaatverandering de armste landen ter wereld schaadt, en hoe ziet compensatie eruit?
Wie is verantwoordelijk als klimaatverandering de armste landen ter wereld schaadt, en hoe ziet compensatie eruit?  Hoe zijn de paden die die planeten rond de zon rond de zon worden genoemd?
Hoe zijn de paden die die planeten rond de zon rond de zon worden genoemd?  Wat is een beschrijving van de oppervlakte -aarde?
Wat is een beschrijving van de oppervlakte -aarde?  Wie ontdekte elliptische banen?
Wie ontdekte elliptische banen?  Hoe een 'manosfeer'-influencer extreme mannelijkheid verkoopt aan jonge mannen
Hoe een 'manosfeer'-influencer extreme mannelijkheid verkoopt aan jonge mannen  Hoeveel soorten chemische bindingen zijn er in ammoniumbromide?
Hoeveel soorten chemische bindingen zijn er in ammoniumbromide?  Aanzetten tot haat is nog steeds gemakkelijk te vinden op sociale media
Aanzetten tot haat is nog steeds gemakkelijk te vinden op sociale media Jurassic Park:waarom we dertig jaar later nog steeds moeite hebben om dit te realiseren
Jurassic Park:waarom we dertig jaar later nog steeds moeite hebben om dit te realiseren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

