
Wetenschap
Wat gebeurt er als u koperchloride verwarmt?
1. Uitdroging:
* cucl 2 • 2h 2 O (gehydrateerd koperchloride) -> CUCL 2 (watervrij koperen chloride) + 2H 2 O (water)
* Dit is de meest voorkomende reactie. Gehydrateerd koperchloride is blauwgroen in kleur. Verwarming drijft zachtjes van de watermoleculen af, waardoor watervrij koperchloride achterblijft, dat geelachtig bruin is.
2. Ontleding:
* cucl 2 (watervrij koperchloride) -> Cucl (koper (i) chloride) + 1/2 CL 2 (chloorgas)
* Bij hogere temperaturen (boven 400 ° C) kan watervrij koperchloride ontleden. Deze reactie geeft chloorgas vrij en laat koper (I) chloride achter, dat wit is.
3. Reactie met zuurstof:
* 2 cucl 2 + O 2 -> 2 cuo (koperoxide) + 2 CL 2 (chloorgas)
* In aanwezigheid van zuurstof kan koperchloride oxideren om koperoxide te vormen. Deze reactie geeft chloorgas vrij.
Belangrijke overwegingen:
* Temperatuur: De temperatuur waarbij deze reacties optreden, varieert. Lagere temperaturen worden meestal gebruikt voor uitdroging, terwijl hogere temperaturen nodig zijn voor ontleding en oxidatie.
* sfeer: De aanwezigheid van zuurstof kan de uitkomst beïnvloeden. Uitdroging kan optreden in een vacuüm of inerte atmosfeer, terwijl oxidatie zuurstof vereist.
* Verwarmingssnelheid: Snelle verwarming kan leiden tot ongecontroleerde reacties en mogelijk gevaarlijke omstandigheden.
Veiligheidsmaatregelen:
* Chloorgas is giftig en corrosief. Alle experimenten met het verwarmen van koperchloride moeten worden uitgevoerd in een goed geventileerd gebied of met behulp van een rookkap.
* Gebruik geschikte veiligheidsapparatuur, inclusief handschoenen, bril en laboratoriumjassen.
Samenvattend: Verwarming koperchloride kan resulteren in uitdroging, ontleding of oxidatie, waardoor verschillende koperen verbindingen en gassen worden geproduceerd. De specifieke reactie en uitkomst zijn afhankelijk van de temperatuur, atmosfeer en andere omstandigheden. Het is essentieel om de juiste veiligheidsmaatregelen te gebruiken bij het hanteren van koperchloride en het uitvoeren van experimenten met verwarming.
 Een nieuw magnetisch materiaal en opnameproces om de datacapaciteit enorm te vergroten
Een nieuw magnetisch materiaal en opnameproces om de datacapaciteit enorm te vergroten Waar staat koolstoftetrahydride voor?
Waar staat koolstoftetrahydride voor?  Heeft zout invloed op de temperatuur van kokend water?
Heeft zout invloed op de temperatuur van kokend water?  Hoe zijn de onderwerpen ionenvorming en periodieke trends met elkaar verbonden?
Hoe zijn de onderwerpen ionenvorming en periodieke trends met elkaar verbonden?  Welke metalen die geen geleider zijn, heeft de elektrische stroom toegestaan?
Welke metalen die geen geleider zijn, heeft de elektrische stroom toegestaan?
 Red onze oceanen om onze gezondheid te beschermen - wetenschappers vragen om een wereldwijd actieplan
Red onze oceanen om onze gezondheid te beschermen - wetenschappers vragen om een wereldwijd actieplan Hoe verschilt de wetenschappelijke rede van andere manieren van denken?
Hoe verschilt de wetenschappelijke rede van andere manieren van denken?  Studie onderzoekt toenemende kans op extreme zeespiegels
Studie onderzoekt toenemende kans op extreme zeespiegels Viruscrisis geeft wegwerpplastic een tweede leven
Viruscrisis geeft wegwerpplastic een tweede leven Ongeveer de helft van de hydraulisch gebroken putten bevindt zich binnen 2 tot 3 kilometer van huishoudelijke grondwatersystemen:studie
Ongeveer de helft van de hydraulisch gebroken putten bevindt zich binnen 2 tot 3 kilometer van huishoudelijke grondwatersystemen:studie
Hoofdlijnen
- Is de Yucca -bloem niet -vasculair of vasculair?
- Wat zijn 2 functies van koolhydraten in cellen?
- Wat zijn belangrijke redenen voor celdeling?
- Wat is een gespecialiseerd gebied van het endoplasmatisch reticulum?
- Wat is menselijke fysiologie?
- Factoren die de groei van micro-organismen beïnvloeden
- Wat is het milieueffect van suiker?
- Welk type plant heeft geen vaatweefsels?
- Evolueren organismen langzaam in de loop van de tijd en kunnen twee verschillende een gemeenschappelijke voorouder hebben?
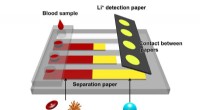
- Nieuw apparaat detecteert snel lithiumionen in bloed van patiënten met bipolaire stoornis
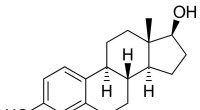
- Oestrogene en anti-oestrogene effecten van PFAS's kunnen afhankelijk zijn van de aanwezigheid van oestrogeen
- Stabiele radicalen kunnen onconventionele problemen in de moderne wetenschap en technologie oplossen

- Nieuw elektronisch apparaat detecteert explosieve dampen

- Onderzoekers ontwikkelen nieuwe behandeling voor botinfectie met koperrijk glasimplantaat

 Wetenschappers leren van rupsen hoe ze zelfassemblerende capsules kunnen maken voor medicijnafgifte
Wetenschappers leren van rupsen hoe ze zelfassemblerende capsules kunnen maken voor medicijnafgifte  Goud bereikt zijn gouden eeuw als hightech materiaal
Goud bereikt zijn gouden eeuw als hightech materiaal Tijdomkeringsasymmetrie overtreft conversie-efficiëntielimiet voor zonnecellen
Tijdomkeringsasymmetrie overtreft conversie-efficiëntielimiet voor zonnecellen Staart zonder komeet:de stoffige overblijfselen van komeet ATLAS
Staart zonder komeet:de stoffige overblijfselen van komeet ATLAS In welke omgeving zou je een chemisch sedimentair gesteente kunnen verwachten?
In welke omgeving zou je een chemisch sedimentair gesteente kunnen verwachten?  Hoeveel aminozuren zitten er in DNA en eiwitten?
Hoeveel aminozuren zitten er in DNA en eiwitten?  Wat biedt de energie voor een koelkast om van binnen naar buiten te gaan?
Wat biedt de energie voor een koelkast om van binnen naar buiten te gaan?  Lichte lagen zanderige as vallen in de buurt van uitbarstende Hawaii-vulkaan
Lichte lagen zanderige as vallen in de buurt van uitbarstende Hawaii-vulkaan
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

