
Wetenschap
Hoe verwijdert calciumhydroxide zwaveldioxide?
1. Contact: Zwaveldioxidegas wordt in contact gebracht met een slurry van calciumhydroxide in water.
2. reactie: Het calciumhydroxide reageert met het zwaveldioxide om calciumsulfiet te vormen (CASO 3 ) en water:
`` `
CA (OH) 2 + So 2 → CASO 3 + H 2 O
`` `
3. neerslag: Het calciumsulfiet, dat is onoplosbaar in water, neerslaat uit de oplossing.
4. Verwijderen: Het neergeslagen calciumsulfiet wordt verzameld en verwijderd, waardoor het zwaveldioxide effectief uit de gasstroom wordt verwijderd.
Voordelen van het gebruik van calciumhydroxide:
* kosteneffectief: Calciumhydroxide is een relatief goedkoop reagens.
* Effectief: Het verwijdert effectief zwaveldioxide uit rookgassen.
* Milieuvriendelijk: De bijproducten van de reactie, calciumsulfiet en water zijn relatief onschadelijk.
Beperkingen:
* Beperkte efficiëntie: Nat schrobben met calciumhydroxide is niet 100% efficiënt. Sommige zwaveldioxide kan aan de scrubber ontsnappen.
* BYproduct Management: Het calciumsulfiet moet goed worden verzameld en verwijderd.
* oxidatie: In aanwezigheid van zuurstof kan calciumsulfiet oxideren tot calciumsulfaat (CASO 4 ), wat moeilijker te verwijderen is.
Toepassingen:
Dit proces wordt veel gebruikt in verschillende industrieën, waaronder:
* Power Plants: Om zwaveldioxide te verwijderen uit rookgassen die worden gegenereerd door het verbranden van fossiele brandstoffen.
* Industriële processen: Om zwaveldioxide uit emissies uit verschillende industriële processen te schrobben.
Opmerking: Dit proces wordt vaak aangeduid als "rookgasontulfurisatie" (FGD) in de context van energiecentrales. Er zijn andere FGD-technologieën die verschillende reagentia en processen gebruiken, maar calciumhydroxide blijft een populaire en kosteneffectieve optie.
 Hoeveel zuurstofatomen zijn aanwezig in het samengestelde molybdenumiii -fosfaat?
Hoeveel zuurstofatomen zijn aanwezig in het samengestelde molybdenumiii -fosfaat?  AI-chemicus synthetiseert katalysator voor zuurstofproductie uit meteorieten op Mars:een stap dichter bij immigratie naar Mars?
AI-chemicus synthetiseert katalysator voor zuurstofproductie uit meteorieten op Mars:een stap dichter bij immigratie naar Mars?  Rijke defecten die de zuurstofontwikkelingsreactie stimuleren
Rijke defecten die de zuurstofontwikkelingsreactie stimuleren Evenwichtige reactie voor de afbraak van water?
Evenwichtige reactie voor de afbraak van water?  Wat is de moleculaire formule van een verbinding als gewichtseenheid 120 en empirische C3H4?
Wat is de moleculaire formule van een verbinding als gewichtseenheid 120 en empirische C3H4?
Hoofdlijnen
- Toyocamycine-opnamewijze ontdekt:goed nieuws voor de ontwikkeling van antischimmelmiddelen
- Wie houdt er van keverspiesjes? Wat Europeanen denken over alternatief eiwitrijk voedsel
- Waarom wordt natuurlijke selectie ook differentiaal of overleving genoemd?
- Bacteriën die geen aerobe ademhaling vereisen?
- Hoe de gezondheid van honingbijenkorven het milieubeleid in Canadese steden kan beïnvloeden
- Welke macromoleculen zijn te vinden in levende wezens?
- Een 'aardbeving' in de cel:wetenschappers ontdekken hoe een wijziging van de nucleaire lamina zijn vorm behoudt
- Wanneer citroenen je leven geven:Herpetofauna-aanpassing aan citrusboomgaarden in Belize
- Het verschil tussen sikkelceltrek en ziekte?
- Nieuwe screeningstechniek om de jacht op kankerbestrijdende medicijnen drastisch te versnellen

- Verkorting van de toeleveringsketen van zeldzame aardmetalen via recycling
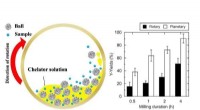
- Ontwikkeling van een 3D-structuur op basis van titanium om botimplantaten te verbeteren

- Kankercellen van patiënten groeien betrouwbaar op nieuwe 3D-steiger, veelbelovend voor precisiegeneeskunde
- Onderzoekers printen kanaalstructuren in kwartsglas

 What Foods Make Electricity?
What Foods Make Electricity?  Waarom wordt het hart nooit moe?
Waarom wordt het hart nooit moe?  Wat zijn de vier soorten luchtmassa?
Wat zijn de vier soorten luchtmassa?  Hoeveel zonne -energie wordt geabsorbeerd en hoe weerspiegeld van het oppervlak?
Hoeveel zonne -energie wordt geabsorbeerd en hoe weerspiegeld van het oppervlak?  Europese technologieleiders waarschuwen voor EU-belasting op digitale diensten
Europese technologieleiders waarschuwen voor EU-belasting op digitale diensten Een nieuw type infrarood polaritonen aan het oppervlak van bulkkristallen
Een nieuw type infrarood polaritonen aan het oppervlak van bulkkristallen Onderzoekers identificeren post-translationele vorming van gespannen cyclofanen in bacteriën
Onderzoekers identificeren post-translationele vorming van gespannen cyclofanen in bacteriën Is etsenglas met zuur een chemische of fysieke verandering?
Is etsenglas met zuur een chemische of fysieke verandering?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

