
Wetenschap
Reactie van aluminiumsulfaat met bariumchloride?
Hier is de evenwichtige chemische vergelijking:
al₂ (So₄) ₃ (aq) + 3bacl₂ (aq) → 3baso₄ (s) + 2alcl₃ (aq)
Verklaring:
* reactanten:
* Aluminiumsulfaat (Al₂ (So₄) ₃) is een oplosbaar zout in water.
* Bariumchloride (BACL₂) is ook oplosbaar in water.
* Producten:
* Bariumsulfaat (Baso₄) is een onoplosbaar zout In water, wat betekent dat het een vast neerslag vormt dat uit oplossing valt.
* Aluminiumchloride (alcl₃) blijft opgelost in oplossing.
Netto ionische vergelijking:
Om ons te concentreren op de soort die direct betrokken is bij de neerslagvorming, kunnen we de netto ionische vergelijking schrijven:
3ba²⁺ (aq) + 3So₄²⁻ (aq) → 3baso₄ (s)
Observaties:
* Wanneer oplossingen van aluminiumsulfaat en bariumchloride worden gemengd, een wit neerslag van bariumsulfaatvormen, waardoor de oplossing bewolkt is.
* De resterende oplossing bevat aluminiumchloride, dat blijft opgelost.
Gebruik:
Deze reactie wordt in verschillende toepassingen gebruikt, waaronder:
* Analytische chemie: om de concentratie sulfaationen in oplossingen te bepalen.
* Industriële processen: bij de productie van bariumsulfaat, gebruikt als een wit pigment in verf en als een vulmiddel in papier.
* Medische procedures: Bariumsulfaat wordt gebruikt als contrastmiddel bij medische beeldvorming, met name röntgenfoto's van het spijsverteringssysteem.
 Wat is de oxidatietoestand van ICL?
Wat is de oxidatietoestand van ICL?  Waarom de oplosbaarheid van jodium in water toeneemt naarmate de concentratie kaliumjodide toeneemt?
Waarom de oplosbaarheid van jodium in water toeneemt naarmate de concentratie kaliumjodide toeneemt?  Waarom exploderen azijn en zuiveringszout als ze met elkaar gemengd worden?
Waarom exploderen azijn en zuiveringszout als ze met elkaar gemengd worden?  Het produceren van foutloze metaalkristallen van ongekende grootte
Het produceren van foutloze metaalkristallen van ongekende grootte Wat is de chemische formule van stikstof in lucht?
Wat is de chemische formule van stikstof in lucht?
 Is er een manier om gratis energie te krijgen?
Is er een manier om gratis energie te krijgen?  Uit onderzoek blijkt dat klimaatverandering 10% heeft toegevoegd aan Ians regenval
Uit onderzoek blijkt dat klimaatverandering 10% heeft toegevoegd aan Ians regenval Beschermde gebieden werken alleen als ze bevatten wat bedreigde soorten nodig hebben
Beschermde gebieden werken alleen als ze bevatten wat bedreigde soorten nodig hebben  Worden zeldzame wilde dieren verhandeld op het darknet?
Worden zeldzame wilde dieren verhandeld op het darknet?  Produceert Gymnosperms bloemen en fruit?
Produceert Gymnosperms bloemen en fruit?
Hoofdlijnen
- Biologische fitheid is het vermogen van individu om?
- Hoe virussen hun gastheercellen te slim af zijn
- Wat zijn de overeenkomsten van dierencellen en planten?
- Waarom is variatie belangrijk voor het overleven van een soort?
- Welke regels moet je volgen als wetenschapper?
- Eenmaal uitgestorven verklaard, Lord Howe Island wandelende takken leven echt
- Wat zijn enkele algemene kenmerken van algen?
- Hoe de landbouw zou kunnen veranderen in een wereld na de groei
- Nature or nurture:zit geweld in onze genen?
- Supercondensator met snoepriet kan snel opladen van mobiele telefoons mogelijk maken
- Chemici helpen kans een handje

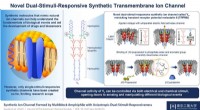
- Dubbel genot:nieuw synthetisch transmembraan-ionkanaal kan op twee manieren worden geactiveerd
- De meest complete studie van batterijstoringen ziet het licht
- Wetenschappers ontwikkelen een nieuwe methode om de efficiëntie van luchtreinigers te verbeteren

 Wat is een andere naam voor afvalsenergie?
Wat is een andere naam voor afvalsenergie?  Hoeveel covalente bindingen worden gevormd door silicium?
Hoeveel covalente bindingen worden gevormd door silicium?  Simpelere tijden:was een eerder genetisch molecuul ouder dan DNA en RNA?
Simpelere tijden:was een eerder genetisch molecuul ouder dan DNA en RNA?  Astronomen zien warme gloed van Uranus-ringen
Astronomen zien warme gloed van Uranus-ringen Hoe bacteriële files leiden tot antibioticaresistente, meerlaagse biofilms
Hoe bacteriële files leiden tot antibioticaresistente, meerlaagse biofilms  De natuurlijke koolstofputten van de aarde hebben een vitale kracht in de strijd tegen het klimaat
De natuurlijke koolstofputten van de aarde hebben een vitale kracht in de strijd tegen het klimaat Het ventrale oppervlak van een zeester wordt genoemd?
Het ventrale oppervlak van een zeester wordt genoemd?  Het lek op wasvervuiling dichten
Het lek op wasvervuiling dichten
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

