
Wetenschap
Hoe deden de eigenschappen van zwavel alleen vergeleken met in het onverwarmde ijzercombinatie?
alleen zwavel:
* uiterlijk: Felgele, brosse vaste stof.
* geur: Karakteristiek, scherp, vaak beschreven als 'rotte eieren'.
* smeltpunt: Relatief laag (115,21 ° C of 239,38 ° F).
* kookpunt: 444.6 ° C (832.3 ° F).
* Reactiviteit: Reageert met veel metalen om sulfiden te vormen.
* elektrische geleidbaarheid: Slechte geleider van elektriciteit.
zwavel in onverwarmde ijzercombinatie:
* uiterlijk: Geen onmiddellijke reactie. Zwavel en ijzer bestaan als afzonderlijke vaste stoffen, met hun individuele eigenschappen.
* geur: Alleen de karakteristieke geur van de zwavel is aanwezig.
* Reactiviteit: Hoewel ijzer en zwavel bij kamertemperatuur kunnen reageren, is het een zeer langzaam proces. De reactiesnelheid is te langzaam om merkbaar te zijn.
Zwavel in verwarmde ijzercombinatie:
* uiterlijk: Wanneer verwarmd, wordt de reactie tussen zwavel en ijzer snel en exotherme (laat warmte vrij). Het mengsel gloeit rood heet en een zwarte vaste stof, ijzersulfide (FES), wordt gevormd.
* geur: De scherpe zwavelgeur is aanvankelijk nog steeds aanwezig, maar het vermindert naarmate de reactie vordert.
* Reactiviteit: De reactie is zeer exotherme en de vrijgegeven warmte kan aanzienlijk zijn.
* elektrische geleidbaarheid: Het resulterende ijzersulfide is een betere geleider van elektriciteit dan pure zwavel.
Belangrijkste verschillen:
* Chemische verandering: Het verwarmen van het mengsel veroorzaakt een chemische reactie, waardoor zwavel en ijzer in een nieuwe verbinding (ijzersulfide) worden getransformeerd.
* Fysieke eigenschappen: Het resulterende ijzersulfide heeft verschillende fysische eigenschappen (kleur, geleidbaarheid, etc.) dan alleen zwavel of ijzer.
* exotherme reactie: De warmte die tijdens de reactie vrijkomt, duidt op een significante energieverandering.
Samenvattend worden de eigenschappen van Sulphur dramatisch gewijzigd in combinatie met ijzer en verwarmd. Het ondergaat een chemische verandering en vormt een nieuwe verbinding met verschillende fysische eigenschappen.
 NASA werpt een infrarood oog op tropische storm Kujiras, zeer koude wolkentoppen
NASA werpt een infrarood oog op tropische storm Kujiras, zeer koude wolkentoppen Verandering van de bodem de sleutel tot het verminderen van blootstelling aan lood bij kinderen
Verandering van de bodem de sleutel tot het verminderen van blootstelling aan lood bij kinderen Klimaatverandering op het zuidelijk halfrond
Klimaatverandering op het zuidelijk halfrond Belangrijke basisinformatie over ijsberen voor kinderen
Belangrijke basisinformatie over ijsberen voor kinderen  Nieuw onderzoek ondersteunt de vulkanische oorsprong van ijzererts van het Kiruna-type
Nieuw onderzoek ondersteunt de vulkanische oorsprong van ijzererts van het Kiruna-type
Hoofdlijnen
- Hoe verhoogt de reproductieve isolatie de diversiteit?
- Nieuw voorspellingsmodel voor kantelpunten biedt inzicht in afnemende bijenvolken
- Wat is de ultieme oorzaak van vooringenomenheid in de wetenschap?
- Hoeveel soorten biomen zijn er?
- Reflecteert Saturnus licht?
- Fossiele of anorganische structuur? Wetenschappers verdiepen zich in vroege levensvormen
- Dit alle soorten straling en cemotherapie Dit medicijn hebben gewoon in de som dagen, maar fulltime die onderzoekers heeft ontdekt, het mogelijk is of niet mogelijk?
- Wat zijn de twee belangrijkste groepen in het koninkrijk van Animalia?
- Wat is de juiste getranscribeerde RNA -streng voor DNA AGC CAA ATG?
- Wetenschappers ontwikkelen mangaanoxidekatalysator met instelbare zuurgraad en selectiviteit

- Kationmenging induceert zeer efficiënte natriumopslag voor gelaagde kathoden
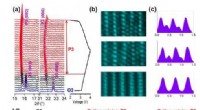
- Onderzoekers ontdekken structuur van anti-verouderingshormoon
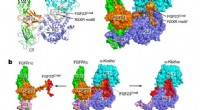
- Onderzoekers benutten de kracht van carbenen om drugs gemakkelijker en veiliger te fabriceren
- Systematische studie lost discussie over katalysatorontwerp voor uitlaatgassen van auto's op

 Hoe maak je een zelfgemaakte magnetische levitatie
Hoe maak je een zelfgemaakte magnetische levitatie Zeehonden versus Walruses
Zeehonden versus Walruses  Hoeveel neutronen bevat een platina -atoom?
Hoeveel neutronen bevat een platina -atoom?  NASA kondigt eerste bemande SpaceX-vlucht aan voor 27 mei
NASA kondigt eerste bemande SpaceX-vlucht aan voor 27 mei Welk kleurloze, geurloze, smaakloze gas adem je in?
Welk kleurloze, geurloze, smaakloze gas adem je in?  Hoe breed is de grootste bekende ster?
Hoe breed is de grootste bekende ster?  Wat kun je in de ruimte zien met een 525X Power Telescope een objectieve diameter van 70 mm?
Wat kun je in de ruimte zien met een 525X Power Telescope een objectieve diameter van 70 mm?  Oekraïne blust bosbrand rond Tsjernobyl
Oekraïne blust bosbrand rond Tsjernobyl
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

