
Wetenschap
Welke massa NO2 wordt gevormd als er geen reageert met 384 g O2?
1. Schrijf de gebalanceerde chemische vergelijking
De reactie tussen NO en O2 produceert NO2:
2 Nee + O2 → 2 No2
2. Bereken de mol O2
* Zoek de molaire massa van O2:16 g/mol (O) * 2 =32 g/mol
* Bereken de mol O2:384 g / 32 g / mol =12 mol
3. Bepaal de mol No2 geproduceerd
* De gebalanceerde vergelijking toont een 1:2 molverhouding tussen O2 en NO2.
* Dit betekent dat voor elke 1 mol O2, 2 mol NO2 wordt geproduceerd.
* Mol No2:12 mol O2 * (2 mol No2 / 1 mol o2) =24 mol NO2
4. Bereken de massa van No2
* Zoek de molaire massa van No2:14 g/mol (n) + 16 g/mol (o) * 2 =46 g/mol
* Bereken de massa van No2:24 mol * 46 g/mol =1104 g
Antwoord: 1104 gram No2 wordt gevormd wanneer er geen reageert met 384 gram O2.
 Schadelijke kleurstoffen in meren, rivieren kunnen kleurloos worden met nieuwe, sponsachtig materiaal
Schadelijke kleurstoffen in meren, rivieren kunnen kleurloos worden met nieuwe, sponsachtig materiaal Elektrisch neutraal radicaal:een sterk chemisch reductiemiddel bij blootstelling aan licht
Elektrisch neutraal radicaal:een sterk chemisch reductiemiddel bij blootstelling aan licht Wat heeft 7 valentie-elektronen in het periodiek systeem?
Wat heeft 7 valentie-elektronen in het periodiek systeem?  Enzym die de chemische afbraak van een stof veroorzaakt?
Enzym die de chemische afbraak van een stof veroorzaakt?  Geavanceerde microscopie onthult ongebruikelijke DNA-structuur
Geavanceerde microscopie onthult ongebruikelijke DNA-structuur
 Plan om droogte in West te bestrijden hangt af van Californië, Arizona
Plan om droogte in West te bestrijden hangt af van Californië, Arizona Hoe kustbossen worden beheerd, kan de watercyclus beïnvloeden
Hoe kustbossen worden beheerd, kan de watercyclus beïnvloeden Canyon in Arizona, beroemd om watervallen die na overstromingen weer opengaan
Canyon in Arizona, beroemd om watervallen die na overstromingen weer opengaan Een halve graad warmer betekent 30, 000 meer doden per jaar in stedelijk China:studie
Een halve graad warmer betekent 30, 000 meer doden per jaar in stedelijk China:studie Brandweerlieden racen om gigantische sequoia's te beschermen bij branden in Californië
Brandweerlieden racen om gigantische sequoia's te beschermen bij branden in Californië
Hoofdlijnen
- Oceaanmonumenten worden geconfronteerd met mogelijk verlies van bescherming
- Hoe wordt een chemische stof gemaakt door klier?
- Elk type cel heeft een specifiek wat?
- Welk woord injecteert DNA of RNA in de kern van een cel om zich voort te planten?
- Hoe worden de eigenschappen niet gemanifesteerd bij ouders die nakomelingen verschijnen?
- Waar worden erytrocyten gesynthetiseerd?
- Veranderingen in mariene ecosystemen blijven onopgemerkt
- Hoe zijn structuur en functie gerelateerd in levende wezens?
- Wat is een selectief permeabel membraan en hoe werkt het?
- Hoe verandert deze blauwe bloementhee van kleur?

- Onderzoekers onderzoeken de invloed van schimmelrot op de aroma's van most en wijn

- Onderzoekers onthullen de aard van het bodemwater en de faseovergang ervan
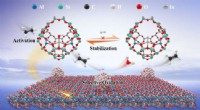
- Onderzoekers passen de katalysator van de hoofdgroep aan met atomair gedispergeerde in-sites voor zeer efficiënte oxidatieve dehydrogenering
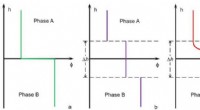
- Symmetrische splitsing van disulfiden is snel en biocompatibel

 Wat is het verschil tussen een positieve en een negatieve reactie in de biologie?
Wat is het verschil tussen een positieve en een negatieve reactie in de biologie?  Waarom wortels niet in de schaduw groeien
Waarom wortels niet in de schaduw groeien  Wat zijn twee acties van korst die een fout kunnen creëren?
Wat zijn twee acties van korst die een fout kunnen creëren?  Welk object weerspiegelt licht?
Welk object weerspiegelt licht?  Hoe gebruikte Newton observatie van de natuur om de bewegingsplaneten te verklaren?
Hoe gebruikte Newton observatie van de natuur om de bewegingsplaneten te verklaren?  Waar zal de richting van de zon het hoogst in de lucht zijn?
Waar zal de richting van de zon het hoogst in de lucht zijn?  Waarom duren planeten verder van de zon langer om een baan om een baan?
Waarom duren planeten verder van de zon langer om een baan om een baan?  Is het ethisch verantwoord om soldaten toe te staan prestatieverhogende medicijnen zoals steroïden te gebruiken?
Is het ethisch verantwoord om soldaten toe te staan prestatieverhogende medicijnen zoals steroïden te gebruiken?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

