
Wetenschap
Waarom hebben de meeste koperen zouten een blauwe kleur?
* koper (ii) ionen elektronische configuratie: Koper (II) heeft een D⁹ -elektronische configuratie, wat betekent dat het één ongepaarde elektron in zijn D -orbitalen heeft.
* Ligand Field Splitting: Wanneer een ligand (zoals water of chloride -ionen) het Cu²⁺ -ion nadert, interageert het met de D -orbitalen, waardoor ze in verschillende energieniveaus worden opgesplitst. Deze splitsing staat bekend als Ligand Field Splitting .
* D-D-overgangen: Het ongepaarde elektron kan energie absorberen en naar een hogere energie -orbitaal springen. Deze absorptie vindt plaats in het zichtbare gebied van het elektromagnetische spectrum, specifiek in de oranje rode golflengten.
* Aanvullende kleur: Omdat het koper (II) ion oranje rood licht absorbeert, de complementaire kleur , dat is blauw , wordt overgedragen en gereflecteerd, waardoor de oplossing zijn karakteristieke blauwe kleur krijgt.
factoren die de kleur beïnvloeden:
* Ligand Type: Verschillende liganden kunnen verschillende graden van ligandveldsplitsing veroorzaken, wat de kleur van het koperzout beïnvloedt. Koper (II) sulfaat (CUSO₄) is bijvoorbeeld lichtblauw in oplossing, terwijl koper (II) chloride (CUCL₂) groenachtig blauw is.
* concentratie: De intensiteit van de blauwe kleur is afhankelijk van de concentratie van de koper (II) ionen.
* oplosmiddel: Het oplosmiddel kan ook de kleur beïnvloeden door de interactie tussen het Cu²⁺ -ion en het ligand te wijzigen.
Uitzonderingen:
Hoewel de meeste koper (II) zouten blauw zijn, zijn er enkele uitzonderingen, zoals:
* koper (i) zouten: Koper (I) zouten (Cu⁺) zijn meestal kleurloos of wit vanwege de gevulde D-orbitalen, die D-D-overgangen voorkomen.
* koperen zouten met sterk gekleurde liganden: Sommige liganden, zoals cyanide of sulfide, kunnen hun eigen sterke kleur hebben, die de kleur van het koperzout kunnen domineren.
Samenvattend is de blauwe kleur van koperen zouten een gevolg van de interactie tussen het koper (II) ion en de omliggende liganden, wat leidt tot D-D-overgangen en de absorptie van bepaalde golflengten van zichtbaar licht.
Hoofdlijnen
- Welke informatie kan niet worden verkregen uit het Human Genome Project?
- Onderzoekers delen een routekaart ter bevordering van duurzame visserij
- Welk type nuclieczuur draagt de codes voor het maken van eiwitten van kern tot ribosoom?
- Over hoeveel menselijke genen zijn er?
- Uitvindingen in 1947
- Welk deel van Shehnai trilt?
- Welke biomoleculen vormen het cytoskelet?
- Mediterrane potvissen vertonen grote variaties in grootte
- Waarom zijn vitamines belangrijk voor enzymen en hoe heet deze relatie?
- Engineering enzymen om plantaardig afval om te zetten in duurzame producten

- Je volgende houten stoel kan plat aankomen en dan drogen in een 3D-vorm

- Nieuw materiaal op cellulosebasis vertegenwoordigt drie sensoren in één

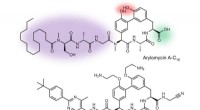
- Gemodificeerde arylomycine blijkt effectief te zijn tegen resistente bacteriën
- Fladderende vleugels aangedreven door de zon

 Wat zijn de kansen om getuige te zijn van een 99 procent zonsverduistering in je leven?
Wat zijn de kansen om getuige te zijn van een 99 procent zonsverduistering in je leven?  Een op ijs geïnspireerd glijmiddel verbetert de symptomen van artrose bij ratten
Een op ijs geïnspireerd glijmiddel verbetert de symptomen van artrose bij ratten Waterkwaliteit:een kwestie van perspectief
Waterkwaliteit:een kwestie van perspectief Is het bouwen van grotere huizen energieverspilling?
Is het bouwen van grotere huizen energieverspilling?  Sociaal netwerk BeReal deelt ongefilterde en onbewerkte momenten uit ons leven - zal het standhouden?
Sociaal netwerk BeReal deelt ongefilterde en onbewerkte momenten uit ons leven - zal het standhouden? Welke cellen hebben gericht?
Welke cellen hebben gericht?  Nieuw mechanisme van supergeleiding ontdekt in grafeen
Nieuw mechanisme van supergeleiding ontdekt in grafeen Hoe zou u de hoeveelheid warmte berekenen die wordt geabsorbeerd of vrijgegeven door een stof wanneer de temperatuur verandert?
Hoe zou u de hoeveelheid warmte berekenen die wordt geabsorbeerd of vrijgegeven door een stof wanneer de temperatuur verandert?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


