
Wetenschap
Is ammoniumfluoride polair of niet -polair?
* Moleculaire vorm: Het ammoniumion (NH₄⁺) heeft een tetraëdrische vorm vanwege de vier waterstofatomen die zijn gebonden aan het stikstofatoom. Het fluoride -ion (F⁻) is een enkel atoom.
* elektronegativiteit: Fluor is het meest elektronegatieve element, wat betekent dat het elektronen sterker aantrekt dan stikstof of waterstof. Dit creëert een significant verschil in elektronegativiteit tussen de stikstof- en fluoratomen in het ammoniumfluoridemolecuul.
* Dipoolmoment: Het ongelijke delen van elektronen tussen stikstof- en fluoratomen creëert een gedeeltelijke negatieve lading op het fluoratoom en een gedeeltelijke positieve lading op het stikstofatoom. Dit creëert een dipoolmoment, dat een scheiding van lading binnen het molecuul aangeeft.
Samenvattend: De asymmetrische vorm van het molecuul en het significante verschil in elektronegativiteit tussen stikstof en fluor resulteert in een netto dipoolmoment, waardoor ammoniumfluoride een polair molecuul is.
 Tijdens abrupte opwarming, kreeften in zuur water hebben een verminderde hartfunctie, minder infectiebestrijdende cellen
Tijdens abrupte opwarming, kreeften in zuur water hebben een verminderde hartfunctie, minder infectiebestrijdende cellen Onderzoek laat zien hoe mosselen omgaan met vervuiling door microplastics
Onderzoek laat zien hoe mosselen omgaan met vervuiling door microplastics Welke vliegende insecten leven in je haar, huid en huis?
Welke vliegende insecten leven in je haar, huid en huis?  Orkanen om kusten een grotere klap te geven
Orkanen om kusten een grotere klap te geven Wereldwijde verviervoudiging van koelapparatuur tot 14 miljard in 2050
Wereldwijde verviervoudiging van koelapparatuur tot 14 miljard in 2050
Hoofdlijnen
- Onderzoek naar fruitvliegen werpt licht op hoe organismen de voedings- en vastencycli reguleren
- Hoe sperma het genoom van vader uitpakt, zodat het kan samensmelten met dat van moeder
- Is een hibiscus dezelfde soort bloem als hippeastrum?
- Is het DNA anders of hetzelfde van de ouder in mitose?
- Wat zijn de voorouders van Cactus?
- Bijna alles over hoe een organisme groeit wordt bepaald door zijn genen?
- Wat is een verschil tussen Desmides en diatomeeën?
- Hoe werkt een vacuole in plantencel?
- Wat zijn de vier DNA -bases met zijn complementaire basis?
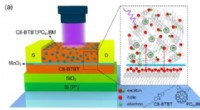
- Wetenschappers ontwikkelen ultragevoelige organische fototransistoren op basis van nieuwe hybride gelaagde architectuur
- Kleurgecodeerd - bijpassende smaak met kleur

- Een nieuw hulpmiddel voor cryo-elektronenmicroscopie

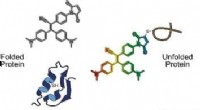
- Moleculaire sonde brengt verkeerd gevouwen proteoomstatus in levende cellen in kaart
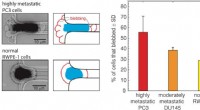
- Nieuwe techniek belooft verbeterde detectie van uitgezaaide prostaatkanker
 Wat 40 miljoen jaar oude tropische rifkoralen ons vertellen over klimaatverandering
Wat 40 miljoen jaar oude tropische rifkoralen ons vertellen over klimaatverandering Wat is rots die in vloeibare vorm smolt?
Wat is rots die in vloeibare vorm smolt?  Waarom is de Mississippi -overstromingsvlakte een van de beste plaatsen om gewassen te laten groeien?
Waarom is de Mississippi -overstromingsvlakte een van de beste plaatsen om gewassen te laten groeien?  Waarom is het principe niet geldig in het geval dat een lift naar boven versnelt, maar het voor een auto op Level Road?
Waarom is het principe niet geldig in het geval dat een lift naar boven versnelt, maar het voor een auto op Level Road?  Is het waar voor de verhalen zoals ze zeggen Izaac Newton?
Is het waar voor de verhalen zoals ze zeggen Izaac Newton?  Wat hebben monomeren en polymeren te maken met fotosynthese?
Wat hebben monomeren en polymeren te maken met fotosynthese?  Multiresistentie tegen antibiotica:waarom bacteriën zo effectief zijn
Multiresistentie tegen antibiotica:waarom bacteriën zo effectief zijn  Hebben we exomanen gevonden of niet?
Hebben we exomanen gevonden of niet?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

