
Wetenschap
Wat is de reactie wanneer ammoniumsulfiet in water wordt gestopt?
(NH₄) ₂so₃ (s) → 2nh₄⁺ (aq) + So₃²⁻ (aq)
Hier is een uitsplitsing:
* (NH₄) ₂SO₃ (s): Ammoniumsulfiet in zijn vaste toestand.
* 2NH₄⁺ (aq): Twee ammoniumionen (NH₄⁺) opgelost in water.
* so₃²⁻ (aq): Eén sulfietion (SO₃²⁻) opgelost in water.
De reactie is omkeerbaar wat betekent dat de opgeloste ionen ook kunnen recombineren om opnieuw vast ammoniumsulfiet te vormen als het water wordt verdampt. Dit proces wordt oplosbaarheidsevenwicht genoemd .
Het is belangrijk op te merken dat ammoniumsulfiet een zwakke basis is . Dit betekent dat het sulfietion (So₃²⁻) in kleine mate met water kan reageren, wat hydroxide -ionen (OH⁻) produceert en de oplossing enigszins basic maakt. De algehele reactie is echter voornamelijk oplossing en dissociatie.
 Klimaat uitgelegd:hoe regelingen voor emissiehandel ons kunnen helpen over te schakelen naar een koolstofvrije toekomst
Klimaat uitgelegd:hoe regelingen voor emissiehandel ons kunnen helpen over te schakelen naar een koolstofvrije toekomst Wetenschapper brengt kooldioxide-emissies voor de hele VS in kaart om de milieubeleidsvorming te verbeteren
Wetenschapper brengt kooldioxide-emissies voor de hele VS in kaart om de milieubeleidsvorming te verbeteren NASA vindt windschering waardoor tropische depressie 10E worstelt
NASA vindt windschering waardoor tropische depressie 10E worstelt Onderzoekers wenden zich tot oesters als schildwachten voor het opsporen van vervuiling
Onderzoekers wenden zich tot oesters als schildwachten voor het opsporen van vervuiling Kenmerken van Typhoons
Kenmerken van Typhoons
Hoofdlijnen
- Voorbeelden van stoffen die gefaciliteerde diffusie gebruiken
- Wetenschappers ontdekken hoe mysterieus 'circulair RNA' wordt gevormd, claimen een verband met spierdystrofie
- Bonobo's en chimpansees:wat onze naaste familieleden ons over mensen vertellen
- Wat kan er gebeuren voor een beperkte genenstroom?
- Kunnen we de capaciteiten van organismen imiteren om waterpatronen te decoderen voor nieuwe technologieën?
- Verwijst naar een ordelijke sequentie van genetisch ontworpen biologische groeiprocessen?
- Waarom gebruiken wetenschappers massa in plaats van gewicht?
- Wat is de betekenis van dermale ostia in zoölogie?
- Waarom vereist chemiososmose een membraan?
- Het toevoegen van een inert polymeer aan plastic zonnecellen zorgt voor een hoog rendement en eenvoudige productie

- Sensoren detecteren ziektemarkers in adem

- Verrassende ontdekking van spinnenhaar kan leiden tot sterkere lijmen
- Door ijzer gemedieerde kankercelactiviteit:een nieuw regulatiemechanisme

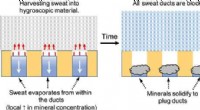
- Het zweet tegen zichzelf keren met een metaalvrije anti-transpirant
 Communicatieapparaat biedt enorm bandbreedtepotentieel
Communicatieapparaat biedt enorm bandbreedtepotentieel Kleine verpakkingen kunnen een krachtige behandeling voor hersentumoren bevatten
Kleine verpakkingen kunnen een krachtige behandeling voor hersentumoren bevatten Hoe scheid je keukenzout, zwavelpoeder en zand uit hun mengsel?
Hoe scheid je keukenzout, zwavelpoeder en zand uit hun mengsel?  Hoe een eenvoudig weerstation te maken
Hoe een eenvoudig weerstation te maken  Nieuwe kaart van Nederland laat zien waar stikstofreductie het meest effectief is
Nieuwe kaart van Nederland laat zien waar stikstofreductie het meest effectief is Welke dosis geothermische betekenen?
Welke dosis geothermische betekenen?  Wat zijn 5 kenmerken die alle mineralen gemeen hebben?
Wat zijn 5 kenmerken die alle mineralen gemeen hebben?  Welk deel van de CO2 die in 1999 in de atmosfeer werd uitgestoten, was afkomstig van de openbare elektriciteits- en warmteproductie?
Welk deel van de CO2 die in 1999 in de atmosfeer werd uitgestoten, was afkomstig van de openbare elektriciteits- en warmteproductie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

