
Wetenschap
Waarom is fluor kleiner dan zuurstof?
Dit is de reden waarom fluor groter is dan zuurstof:
* Effectieve nucleaire lading: Fluor heeft nog één proton dan zuurstof, wat leidt tot een sterkere aantrekkingskracht tussen de kern en elektronen. Deze sterkere aantrekkingskracht kan ertoe leiden dat fluor *kleiner *zou zijn *.
* Regeling van elektronen-elektronen: Zowel fluor als zuurstof hebben echter een volledige buitenste schaal van elektronen (2S²2P⁵). Dit betekent dat er in fluor meer elektron-elektronenafstoting is vanwege het extra elektron. Deze afstoting duwt de elektronen verder uit elkaar en verhoogt de atoomradius.
In wezen, terwijl fluor een sterkere trek heeft van de kern, weegt de verhoogde elektron-elektronenafstoting op tegen dit effect, waardoor fluor groter is dan zuurstof.
Laat het me weten als je andere periodieke trends wilt verkennen!
 Uit onderzoek blijkt hoe afval kan worden omgezet in materialen voor geavanceerde industrieën
Uit onderzoek blijkt hoe afval kan worden omgezet in materialen voor geavanceerde industrieën  Welke verandering van het oppervlak wanneer vers gesneden lithiummetaal reageert met lucht?
Welke verandering van het oppervlak wanneer vers gesneden lithiummetaal reageert met lucht?  Waarom is mijnbouw van metaal slecht?
Waarom is mijnbouw van metaal slecht?  Bestaat Compound uit waterstof of zuurstof?
Bestaat Compound uit waterstof of zuurstof?  Hoeveel eenzame paren elektronen zijn er in een stikstofmolecuul?
Hoeveel eenzame paren elektronen zijn er in een stikstofmolecuul?
 Onderzoek naar grondfalen toont aan dat diepe aardverschuivingen niet zijn gereactiveerd tegen Anchorage Quake in 2018
Onderzoek naar grondfalen toont aan dat diepe aardverschuivingen niet zijn gereactiveerd tegen Anchorage Quake in 2018 Koolstofkredieten zouden het herstel van Britse kwelders mogelijk maken, zeggen experts
Koolstofkredieten zouden het herstel van Britse kwelders mogelijk maken, zeggen experts  Voordelen & nadelen van woestijnen
Voordelen & nadelen van woestijnen Die geuren waar je van houdt? Dinosaurussen vonden ze het eerst leuk
Die geuren waar je van houdt? Dinosaurussen vonden ze het eerst leuk  Land kan ongeveer een kwart van de maandelijkse neerslag vasthouden
Land kan ongeveer een kwart van de maandelijkse neerslag vasthouden
Hoofdlijnen
- Hoe natuurkunde en biologie samenwerken om de mechanismen van het leven te verkennen
- Waarom bestaan er wetenschappelijke modellen?
- Welk type populatie zou de evolutie het snelst optreden?
- Wat is de actie van eencellige organismen die in een vijver leven?
- Welk type weefsellijnen de nasopharynx?
- Welke twee bollen komen chemicaliën in de ecosystemen?
- Wat zijn de aanpassingen van een lelie?
- Hoeveel cellen houd je over na mitose en meiose?
- Wat schadelijk van bacteriën?
- Nieuwe screeningstechniek om de jacht op kankerbestrijdende medicijnen drastisch te versnellen

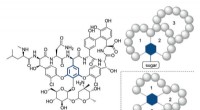
- Eenvoudige éénpotssynthese van medicamenteuze tricyclische peptiden
- Video:De chemie van gebakken kip

- ORNL bereikt belangrijke FDA-mijlpaal voor kankerbestrijdende Ac-225-isotoop
- Afbeelding:Plastic sparrenbos

 Welke omstandigheden kunnen hydrolyse van een ester produceren?
Welke omstandigheden kunnen hydrolyse van een ester produceren?  Australië verlaagt vooruitzichten voor Great Barrier Reef naar zeer slecht
Australië verlaagt vooruitzichten voor Great Barrier Reef naar zeer slecht Wat zijn de voordelen van Planet Go 1214B?
Wat zijn de voordelen van Planet Go 1214B?  Wat is een synoniem voor massale uitsterven?
Wat is een synoniem voor massale uitsterven?  Hoe wordt 134 picometers in meters uitgedrukt?
Hoe wordt 134 picometers in meters uitgedrukt?  Welke actie zal een vaste opgeloste stof langzamer oplossen in vloeibaar oplosmiddel?
Welke actie zal een vaste opgeloste stof langzamer oplossen in vloeibaar oplosmiddel?  Verdringt zwavel waterstof bij reactie met verdunde minerale zuren?
Verdringt zwavel waterstof bij reactie met verdunde minerale zuren?  Welk gebruik maken tieners van YouTube?
Welk gebruik maken tieners van YouTube?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

