
Wetenschap
Wat gebeurt er als zilver wordt toegevoegd aan kopersulfaatoplossing?
* zilver is reactiever dan koper. Dit betekent dat zilver een sterkere neiging heeft om elektronen te verliezen en positieve ionen te vormen (Ag⁺).
* koperionen (cu²⁺) in de oplossing worden aangetrokken door het zilver. De zilveren atomen doneren elektronen aan de koperionen, waardoor ze worden teruggebracht tot koperatomen (Cu).
* zilverionen (Ag⁺) worden gevormd. De zilveren atomen die elektronen doneren worden zilverionen.
* De oplossing verandert van kleur. De blauwe kleur van de kopersulfaatoplossing vervaagt als koperionen worden verwijderd en de oplossing kan enigszins bewolkt worden naarmate koperen metaal neerslaat.
Hier is de chemische vergelijking:
2ag (s) + cuso₄ (aq) → cu (s) + ag₂so₄ (aq)
in eenvoudiger termen:
* Zilver (Ag) verplaatst koper (Cu) van de kopersulfaatoplossing.
* Zilver vormt zilveren sulfaat (Ag₂so₄) die oplost in de oplossing.
* Kopermetaal (Cu) gaat uit de oplossing als een roodbruine vaste stof.
Key Observations:
* Vorming van een roodbruine vaste stof (koperen metaal)
* vervaging van de blauwe kleur van de kopersulfaatoplossing
* Mogelijke lichte bewolking in de oplossing
 Het effect van azijn op kippenbotten
Het effect van azijn op kippenbotten  Wat zijn de gassen die kunnen worden gebruikt als brandstoffen?
Wat zijn de gassen die kunnen worden gebruikt als brandstoffen?  Welke reeks elementen is gerangschikt in volgorde van een afnemende atoomradius?
Welke reeks elementen is gerangschikt in volgorde van een afnemende atoomradius?  Verbeterde chemische verwering:een oplossing voor de klimaatcrisis?
Verbeterde chemische verwering:een oplossing voor de klimaatcrisis?  Wat is de reactie waarbij waterstof wordt verbrand?
Wat is de reactie waarbij waterstof wordt verbrand?
 Onderzoek voorspelt een milieuramp als gevolg van de verwijdering van menstruatieproducten in India
Onderzoek voorspelt een milieuramp als gevolg van de verwijdering van menstruatieproducten in India Hoe zou een sterk klimaatpact eruit zien?
Hoe zou een sterk klimaatpact eruit zien?  Cruiseschepen herstarten in Venetië, breng milieuprotesten
Cruiseschepen herstarten in Venetië, breng milieuprotesten Mijnafvaldammen bedreigen het milieu, zelfs als ze niet falen
Mijnafvaldammen bedreigen het milieu, zelfs als ze niet falen Hoe is een geschenk van land dat wordt genoemd?
Hoe is een geschenk van land dat wordt genoemd?
Hoofdlijnen
- Japanse dierentuin rouwt om dood van verliefde pinguïn
- Superbugs gevonden op Olympische zwemplekken in Rio
- 'Evolutionaire fitheid' speelt een sleutelrol bij het bepalen waarom sommige vrouwen fysiek aantrekkelijker zijn dan andere
- Deskundigen adviseren om benchmarking te gebruiken om bedrijven met een hoog antibioticagebruik te identificeren
- DNA -replicatie treedt op met of zonder de hulp van enzymen?
- Het oplossen van de evolutionaire geschiedenis van de naaste verwanten van algen van landplanten
- Wat zijn bèta -deeltjes?
- Waarom heeft het aërobe metabolisme een voordeel ten opzichte van het anaërobe metabolisme bij levende wezens?
- Wat zijn de verschillen tussen biologisch en fylogenetisch concept van morfologische soorten?
- Duurzamere geuren creëren met biotech

- Chemici synthetiseren ultrasnelle cyanidedetector

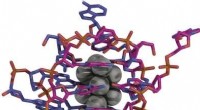
- Bepaling van de kristalstructuur van een DNA-gestabiliseerd zilveren nanocluster
- Nieuwe theorie ontsluit het geheim achter eiwit-membraan-interacties

- Opladen in de toekomst - nieuw steenzout voor gebruik in oplaadbare magnesiumbatterijen

 Waar groeit de mos?
Waar groeit de mos?  Welke bacteriën eten de leukocyten?
Welke bacteriën eten de leukocyten?  Waarom vormt condensatie zich op een drinkglas?
Waarom vormt condensatie zich op een drinkglas?  Hoe klimaatverandering het immuunsysteem van koraal verzwakt
Hoe klimaatverandering het immuunsysteem van koraal verzwakt Hoe chemische vervuiling te voorkomen
Hoe chemische vervuiling te voorkomen Welke gassen maken de Atoshere samen?
Welke gassen maken de Atoshere samen?  Hoe beïnvloedt de winning van steengroeven de bodemerosie?
Hoe beïnvloedt de winning van steengroeven de bodemerosie?  Verbetering van moleculaire beeldvorming met behulp van een diepgaande leerbenadering
Verbetering van moleculaire beeldvorming met behulp van een diepgaande leerbenadering
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

