
Wetenschap
Hoe kunt u het verschil zien tussen amoniumchloride en zilveren chloride?
1. Uiterlijk:
* ammoniumchloride: Wit, kristallijne vaste stof. Het wordt vaak gevonden in kleine, korrelige vorm.
* zilveren chloride: Wit, curdy neerslag. Het vormt zich als een vaste stof wanneer zilverionen reageren met chloride -ionen in oplossing.
2. Oplosbaarheid:
* ammoniumchloride: Zeer oplosbaar in water. Het lost gemakkelijk op om een duidelijke oplossing te vormen.
* zilveren chloride: Onoplosbaar in water. Het blijft als een vast neerslag, zelfs wanneer het wordt gemengd met water.
3. Reactie met warmte:
* ammoniumchloride: Ontbindt bij het verwarmen, het vrijgeven van ammoniakgas (NH₃) en waterstofchloridegas (HCL). Je zult een scherpe geur opmerken.
* zilveren chloride: Smelt bij hoge temperaturen en kan worden afgebroken door sterk licht. Het wordt donker bij blootstelling aan licht.
4. Chemische tests:
* zilveren chloride:
* reactie met salpeterzuur: Zal oplossen in geconcentreerd salpeterzuur.
* reactie met ammoniak: Lost op in geconcentreerde ammoniakoplossing om een complexe ion te vormen.
* ammoniumchloride:
* reactie met natriumhydroxide: Zal ammoniakgas (NH₃) vrijgeven, die een karakteristieke scherpe geur heeft.
BELANGRIJKE VEILIGHEID OPMERKING:
Vergeet niet bij het werken met ammoniumchloride of zilverchloride, vergeet niet om passende veiligheidsuitrusting te dragen, zoals handschoenen en oogbescherming.
Als u niet zeker bent over de identiteit van een stof, probeer er dan niet mee te experimenteren. Raadpleeg een gekwalificeerde chemicus voor identificatie en veilige hantering.
 Wat is de relatie tussen ecologisch en opvolgingsevenwicht in een ecosysteem?
Wat is de relatie tussen ecologisch en opvolgingsevenwicht in een ecosysteem?  2023 was de heetste zomer in 2000 jaar, zo blijkt uit onderzoek
2023 was de heetste zomer in 2000 jaar, zo blijkt uit onderzoek  Grafieken over klimaatverandering zijn belangrijk:maak ze eenvoudig, zeggen experts
Grafieken over klimaatverandering zijn belangrijk:maak ze eenvoudig, zeggen experts  Er zijn dringend nieuwe regels nodig om onze oceanen te beschermen, wetenschappers waarschuwen
Er zijn dringend nieuwe regels nodig om onze oceanen te beschermen, wetenschappers waarschuwen Eeuwig stinkende stad? De afvalcrisis in Rome wekt gezondheidsangst op
Eeuwig stinkende stad? De afvalcrisis in Rome wekt gezondheidsangst op
Hoofdlijnen
- Onderzoekers leggen uit hoe slangen in een rechte lijn kunnen kruipen
- Welk molecuul kruist een celmembraan vaker dan elke andere stof?
- Waar worden organellen gevonden?
- Wat zijn de twee delen van het skeletstelsel?
- Wat is een basisprincipe van kinesiologie?
- Effecten van mobiele telefoons op studenten
- Wat is het proces waarbij DNA zichzelf reproduceert?
- Houden virussen zeeluizen bij wilde zalm op afstand?
- Dengue Achilleshiel inzicht biedt hoop op betere vaccins
- Ontdekking van bacteriële enzymactiviteit kan leiden tot nieuwe op suiker gebaseerde medicijnen
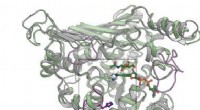
- Verhoogde bruikbaarheid en precisie bij vasculaire beeldvorming
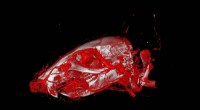
- De volgende generatie katalysatoren ontdekken

- Mangaan aanwerven om koolstofdioxide op te waarderen
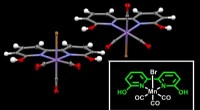
- Hoe kathodische corrosie van metaalelektroden bij elektro-organische synthese te voorkomen?

 Te ingewikkeld denken? Neuronale activiteit is veel voorspelbaarder dan aangenomen
Te ingewikkeld denken? Neuronale activiteit is veel voorspelbaarder dan aangenomen  Wat zijn de 3 principes van de celtheorie?
Wat zijn de 3 principes van de celtheorie?  Bevers hebben invloed op het klimaat
Bevers hebben invloed op het klimaat Wetenschapsprojecten over regenbogen
Wetenschapsprojecten over regenbogen  Hoeveel elektronen zijn er in chloor?
Hoeveel elektronen zijn er in chloor?  Wat is de locatie van 105 graden East en 12 North?
Wat is de locatie van 105 graden East en 12 North?  Hoe snel kan een raket gaan?
Hoe snel kan een raket gaan?  Wat gebeurt er als de aarde rechtstreeks tussen maan en zon is?
Wat gebeurt er als de aarde rechtstreeks tussen maan en zon is?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

