
Wetenschap
Beschrijf de binding in een kristal van jodium?
binding in jodiumkristal:
Jodiumkristallen vertonen A niet -polaire covalente binding Binnen elk jodiummolecuul (i 2 ) en van der Waals krachten tussen deze moleculen. Laten we het afbreken:
1. Covalente binding binnen i 2 :
* Jodiumatomen delen elektronen om een enkele covalente binding te vormen, waardoor hun octet wordt voltooid.
* Deze binding is nonpolar Omdat beide jodiumatomen dezelfde elektronegativiteit hebben, wat resulteert in een gelijk delen van elektronen.
2. Van der Waals krachten tussen i 2 Moleculen:
* De i 2 Moleculen zelf worden bij elkaar gehouden door London Dispersion Forces , een type van der Waals Force.
* Deze krachten komen voort uit tijdelijke schommelingen in elektronenverdeling binnen de moleculen, waardoor tijdelijke dipolen ontstaan.
* Deze geïnduceerde dipolen trekken elkaar aan, waardoor een zwakke intermoleculaire kracht ontstaat.
Algemeen bindingsfoto:
* Elk jodiumatoom vormt een sterke covalente binding met een ander jodiumatoom om een i 2 te vormen molecuul.
* Deze moleculen worden vervolgens zwak bij elkaar gehouden door dispersiekrachten in Londen en vormen een kristallijne structuur.
Key -kenmerken van jodiumkristallen als gevolg van binding:
* vast bij kamertemperatuur: Vanwege de relatief sterke Van der Waals -krachten bestaat jodium als een vaste stof.
* Sublimable: De zwakke intermoleculaire krachten zorgen ervoor dat jodium gemakkelijk overstapt van vast naar gas, wat sublimatie vertoont.
* Slechte warmtegeleider en elektriciteit: De covalente bindingen binnen de i 2 Moleculen zijn sterk, maar de zwakke intermoleculaire krachten resulteren in een slechte geleidbaarheid.
* Glanzende, donkergrijze kleur: Dit is een gevolg van het vermogen van het molecuul om zichtbaar licht te absorberen, met uitzondering van violet licht, dat wordt weerspiegeld.
Samenvattend is de binding in jodiumkristallen een combinatie van sterke covalente bindingen binnen elk jodiummolecuul en zwakke van der Waals -krachten tussen hen. Dit samenspel van krachten geeft jodium zijn karakteristieke fysieke eigenschappen.
 Welke twee lichaamssystemen verwijderen koolstofdioxide uit het lichaam?
Welke twee lichaamssystemen verwijderen koolstofdioxide uit het lichaam?  In welke elementen vervalt uranium 235?
In welke elementen vervalt uranium 235?  Wat is het aantal ongepaarde elektronen in een lithiumatoom?
Wat is het aantal ongepaarde elektronen in een lithiumatoom?  27,0 ml 0,45 m naoh wordt geneutraliseerd door 20 an hcl-oplossing, de molariteit is?
27,0 ml 0,45 m naoh wordt geneutraliseerd door 20 an hcl-oplossing, de molariteit is?  Wanneer er een binding ontstaat, hoeveel valentie-elektronen zijn er dan nodig om een octet te vullen?
Wanneer er een binding ontstaat, hoeveel valentie-elektronen zijn er dan nodig om een octet te vullen?
 Welke effecten hebben chloorfluorkoolstoffen op mensen?
Welke effecten hebben chloorfluorkoolstoffen op mensen?  Onderzoeken waarom planten vroeg bloeien in een opwarmende wereld
Onderzoeken waarom planten vroeg bloeien in een opwarmende wereld  Onderzoekers onderzoeken erosie en veerkracht van rivieroevers aan de kust van Bangladesh
Onderzoekers onderzoeken erosie en veerkracht van rivieroevers aan de kust van Bangladesh Waarom krijgen herten velvet op hun hoorns?
Waarom krijgen herten velvet op hun hoorns?  100 miljoen jaar oude fossielen en zwaartekrachtsgolfwetenschap gebruiken om het toekomstige klimaat op aarde te voorspellen
100 miljoen jaar oude fossielen en zwaartekrachtsgolfwetenschap gebruiken om het toekomstige klimaat op aarde te voorspellen
Hoofdlijnen
- Slechts een derde van het gepubliceerde psychologische onderzoek is betrouwbaar – wat nu?
- Welk deel van het chromosoom is spindelapparaten bevestigd?
- Hoe heet een slijmproductieve cel?
- Wat doet ethanol in een DNA-extractie?
- Leven in drijfhout in zee:het geval van drijfhoutspecialist talitrids
- Hoe worden de 2 belangrijkste takken van de wetenschap genoemd?
- Onderzoekers bepalen hoe groepen beslissingen nemen
- Hoe reproduceert Gladiolus zich?
- Waarom is osmose belangrijk voor de celfunctie?
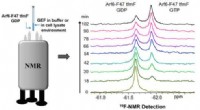
- Snelle methode helpt bij het detecteren van Arf6-guanine-nucleotide-uitwisselingsfactoractiviteit
- Onderzoekers ontwikkelen taaie, zelfherstellend rubber

- Wetenschappers kijken naar vetmetabolisme in levende vissen, observeer real-time lipidenbiochemie
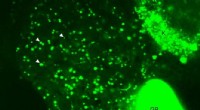
- 3D-geprint apparaat vindt naald in hooiberg kankercellen door hooi te verwijderen

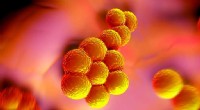
- Tekeneiwit helpt antibiotica MRSA-superbug te bestrijden
 Wat heeft Aurora Borealis met de noordenwind te maken?
Wat heeft Aurora Borealis met de noordenwind te maken?  Wat zijn feiten over de lagen van de aarde?
Wat zijn feiten over de lagen van de aarde?  Wat is de pH van eieren?
Wat is de pH van eieren?  Robots nemen 20 miljoen banen over, toenemende ongelijkheid:studie
Robots nemen 20 miljoen banen over, toenemende ongelijkheid:studie Fluviatiele kartering van Mars
Fluviatiele kartering van Mars Is waterdamp een mengsel of een zuivere stof?
Is waterdamp een mengsel of een zuivere stof?  Waarom wordt mijn huis overspoeld door pantrymotten en hoe kom ik van ze af?
Waarom wordt mijn huis overspoeld door pantrymotten en hoe kom ik van ze af? Silicium golfgeleiders brengen ons dichter bij sneller, op licht gebaseerde logische circuits
Silicium golfgeleiders brengen ons dichter bij sneller, op licht gebaseerde logische circuits
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

