
Wetenschap
Hoeveel natriumionen in 6,2 gram na2o?
1. Bereken de molaire massa van Na₂o:
* NA:22,99 g/mol (atomaire natriummassa)
* O:16,00 g/mol (atomaire zuurstofmassa)
* Molaire massa van Na₂o =(2 * 22,99) + 16.00 =61,98 g/mol
2. Bereken het aantal mol na₂o:
* Mol =massa / molaire massa
* Mol na₂o =6,2 g / 61,98 g / mol =0,100 mol
3. Bepaal het aantal mol natriumionen:
* Elke mol na₂o bevat 2 mol natriumionen (uit de chemische formule).
* Mol na⁺ =0,100 mol na₂o * (2 mol Na⁺ / 1 mol Na₂o) =0.200 mol Na⁺
4. Bereken het aantal natriumionen:
* Gebruik het nummer van Avogadro (6.022 x 10²³ ionen/mol)
* Aantal NA⁺ -ionen =0.200 mol * 6.022 x 10²³ ionen/mol = 1,20 x 10²³ Natriumionen
Daarom zijn er ongeveer 1,20 x 10²³ natriumionen in 6,2 gram na₂o.
 Wanneer is het watermolecuul tijdens de lichte reactie split?
Wanneer is het watermolecuul tijdens de lichte reactie split?  Waarom worden alkalai -metalen gevonden als verbindingen?
Waarom worden alkalai -metalen gevonden als verbindingen?  Hoe zeg je dat ik in het Spaans naar de chemie ga?
Hoe zeg je dat ik in het Spaans naar de chemie ga?  Waarom is de juiste chemische formule voor ijzeroxide?
Waarom is de juiste chemische formule voor ijzeroxide?  Hoe gebruik je de Gibbs Free Energy -vergelijking om verandering te vinden voor de vorming van ammoniak op 25 graden C?
Hoe gebruik je de Gibbs Free Energy -vergelijking om verandering te vinden voor de vorming van ammoniak op 25 graden C?
 Kwetsbaarheid voor klimaatverandering wapenen:tegenmaatregelen treffen de armen vaak
Kwetsbaarheid voor klimaatverandering wapenen:tegenmaatregelen treffen de armen vaak Wetenschappers voorspelden eind mei een tornado-uitbraak, bijna vier weken voordat deze door de VS raasde.
Wetenschappers voorspelden eind mei een tornado-uitbraak, bijna vier weken voordat deze door de VS raasde. Aandachtspunt voor klimaatverandering staat aan de top van onze wereld, en agenda
Aandachtspunt voor klimaatverandering staat aan de top van onze wereld, en agenda Wijnmaken in de Scandinavische landen, een wereld verwijderd van Frans chateau luxe
Wijnmaken in de Scandinavische landen, een wereld verwijderd van Frans chateau luxe Een nieuwe methode om de bestuurders van waterdiefstal beter te begrijpen
Een nieuwe methode om de bestuurders van waterdiefstal beter te begrijpen
Hoofdlijnen
- Wat is het tweede niveau van organisatie in een meercellulair organisme?
- Welke wetenschapper geïsoleerd DNA voor het eerst?
- Wie heeft het nucleaire model ontdekt?
- Onderzoekers kijken naar de fruitvlieg om het menselijk brein te begrijpen
- Hoe noem je een organisme met kern?
- Hoe komen vogels bijeen? Onderzoekers doen de wiskunde om voorheen onbekende aerodynamische fenomenen te onthullen
- Wat is de meest logische volgorde van stappen voor het splitsen van vreemd DNA?
- Hoe een moleculaire schaar op de juiste plaats knipt
- Waarom moet je weten dat biologie een dierenarts is?
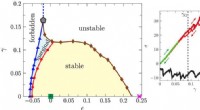
- De fasestabiliteit van zachte materie voorspellen

- Zijn amorfe vaste stoffen elastisch of plastisch?
- Hoe zuurstof de kern van belangrijke enzymen vernietigt

- Nieuwe synthesemethoden verbeteren de chemische 3D-ruimte voor het ontdekken van geneesmiddelen
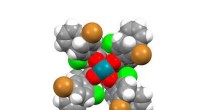
- Vormverschuivende protocellen duiden op de mechanica van het vroege leven

 Planetaire nevel IPHASX J191104.8+060845 in detail onderzocht
Planetaire nevel IPHASX J191104.8+060845 in detail onderzocht Inchworm Levenscyclus
Inchworm Levenscyclus  Astrofysici simuleren een vage galactische halo van donkere materie
Astrofysici simuleren een vage galactische halo van donkere materie Verschil tussen kwartsiet en graniet
Verschil tussen kwartsiet en graniet  Waarom voorkomt dat sterren instorten onder de kracht van hun eigen zwaartekracht?
Waarom voorkomt dat sterren instorten onder de kracht van hun eigen zwaartekracht?  Upconversion-gebaseerde nanosensor ontwikkeld voor detectie van geneesmiddelen voor chemotherapie
Upconversion-gebaseerde nanosensor ontwikkeld voor detectie van geneesmiddelen voor chemotherapie Wat zal er hoogstwaarschijnlijk gebeuren met een plant die niet genoeg CO2 ontvangt?
Wat zal er hoogstwaarschijnlijk gebeuren met een plant die niet genoeg CO2 ontvangt?  Natuurkundige voorspellingen voor fracking en brandstoffen
Natuurkundige voorspellingen voor fracking en brandstoffen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

