
Wetenschap
Waarom wordt natrium in een inerte oplosmiddel gehouden?
1. Reactiviteit met lucht: Natrium is zeer reactief met zuurstof en vocht in de lucht.
* Het reageert met zuurstof om natriumoxide (Na₂o) te vormen, een witte vaste stof.
* Het reageert met water om natriumhydroxide (NaOH) en waterstofgas (H₂) te vormen. Deze reactie is exotherme en kan explosief zijn.
2. Reactiviteit met water: Zelfs kleine hoeveelheden water kunnen ertoe leiden dat natrium gewelddadig reageert. Het geproduceerde waterstofgas kan ontbranden, wat een brand of explosie veroorzaakt.
3. Reactiviteit met andere stoffen: Natrium is ook reactief met veel andere stoffen, zoals zuren, halogenen en alcoholen.
Inerte oplosmiddelen zoals kerosine of minerale olie:
* Voorkom contact met lucht en vocht: Deze oplosmiddelen zijn niet-polair en reageren niet met natrium, waardoor er een beschermende laag omheen wordt gevormd.
* NIET-FALBABLE: In tegenstelling tot andere oplosmiddelen zoals ether of alcohol, zijn kerosine en minerale olie niet brandbaar, waardoor het risico op brand wordt verminderd.
* Lage reactiviteit: Ze zijn relatief inert en reageren niet met natrium en zorgen voor de stabiliteit ervan.
Samenvattend: Natrium in inerte oplosmiddelen zoals kerosine of minerale olie houden, beschermt het tegen het reageren met het milieu, het voorkomen van potentiële gevaren en het behouden van de chemische eigenschappen.
 Team laat zien hoe rivieren kruipen en stromen om landschappen in de loop van de tijd vorm te geven
Team laat zien hoe rivieren kruipen en stromen om landschappen in de loop van de tijd vorm te geven  Door de koolstofemissies van veengebieden te meten, kan de klimaatimpact van ontwikkeling worden gemeten
Door de koolstofemissies van veengebieden te meten, kan de klimaatimpact van ontwikkeling worden gemeten Schaamte of hoop? Hoe moeten we ons voelen over de klimaatverandering?
Schaamte of hoop? Hoe moeten we ons voelen over de klimaatverandering?  Arctisch onderzoek om licht te werpen op organismen die essentieel zijn voor de voedselketen
Arctisch onderzoek om licht te werpen op organismen die essentieel zijn voor de voedselketen Olie uit zeewater verwijderen
Olie uit zeewater verwijderen
Hoofdlijnen
- Hoe boa's zichzelf behoeden voor verstikking tijdens het insnoeren en verteren van het avondeten
- Onderzoekers onthullen nieuwe inzichten in de controle van cellulaire steigers
- Het overdrachtspotentieel van vliegen kan groter zijn dan gedacht, onderzoekers zeggen:
- Wat is de evolutietheorie door natuurlijke selectie?
- Wat denk je dat een enzym zoals DNA -polymerase zou doen?
- Wat zijn de reactanten en producten voor aërobe cellulaire ademhaling?
- Op het spoor van de mondiale klimaatverandering – vulkanisme als aanjager van het klimaat tijdens de Carnische Crisis
- Wat zijn voorbeelden van symbiose -concurrentie en predatie in organismen?
- Wat zijn de twee kenmerken van zoogdieren?
- Een sterker geleidend keramiek tegen lagere kosten
- Video:De kunst en wetenschap van glasblazen

- Wetenschappers gebruiken nieuwe technologieën om water te zien als nooit tevoren

- Met grafeen gewikkelde zeolietmembranen voor snelle waterstofscheiding

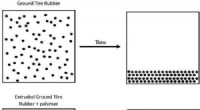
- Polymeren effenen de weg voor een breder gebruik van gerecyclede banden in asfalt
 Wat betekent op afstand gerelateerd?
Wat betekent op afstand gerelateerd?  Welke Amerikaanse staatskapitaal bevindt zich langs een kustlijn van de oceaan?
Welke Amerikaanse staatskapitaal bevindt zich langs een kustlijn van de oceaan?  Welke planeet was misschien ooit een maan van Neptunus.
Welke planeet was misschien ooit een maan van Neptunus.  Onderzoek toont aan hoe gletsjeralgen een donkere zone creëren aan de randen van de Groenlandse ijskap
Onderzoek toont aan hoe gletsjeralgen een donkere zone creëren aan de randen van de Groenlandse ijskap  Waar bestaat rioolwater voornamelijk uit?
Waar bestaat rioolwater voornamelijk uit?  De grootste dataset voor het zoutgehalte van het zeeoppervlak tot nu toe helpt onderzoekers om zoute wateren in kaart te brengen
De grootste dataset voor het zoutgehalte van het zeeoppervlak tot nu toe helpt onderzoekers om zoute wateren in kaart te brengen Door klimaat gedreven extreem weer bedreigt oude bruggen met instorting
Door klimaat gedreven extreem weer bedreigt oude bruggen met instorting Veranderen de absolute posities van maan en aardezon als banen de aarde?
Veranderen de absolute posities van maan en aardezon als banen de aarde?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

