
Wetenschap
Waarom binden natrium- en chloride -ionen zich aan elkaar?
* natrium (na) is een metaal en heeft één valentie -elektron (elektron in de buitenste schaal). Het verliest gemakkelijk dit elektron om een stabiele elektronenconfiguratie te bereiken en wordt een positief geladen natriumion (Na+).
* chloor (Cl) is een niet -metaal en heeft zeven valentie -elektronen. Het heeft nog een elektron nodig om zijn buitenste schaal te voltooien en een stabiele configuratie te bereiken. Het krijgt een elektron van een ander atoom en wordt een negatief geladen chloride-ion (Cl-).
* Tegengestelde ladingen trekken aan: Het positief geladen natriumion (Na+) en het negatief geladen chloride-ion (Cl-) worden tot elkaar aangetrokken vanwege hun tegengestelde ladingen. Deze elektrostatische aantrekkingskracht is wat hen bij elkaar houdt in een ionische binding.
in eenvoudiger termen: Stel je twee magneten voor met tegengestelde palen. Ze blijven natuurlijk bij elkaar vanwege hun tegengestelde aanklachten. Natrium- en chloride -ionen werken op dezelfde manier en vormen een sterke binding vanwege hun tegengestelde ladingen.
Deze ionische binding resulteert in de vorming van natriumchloride (NaCl) , die algemeen bekend staat als tafelzout.
 Review:Bill Gates biedt een hoopvolle kijk op klimaatverandering
Review:Bill Gates biedt een hoopvolle kijk op klimaatverandering De plasticafvalcrisis is een kans voor de VS om thuis serieus te gaan recyclen
De plasticafvalcrisis is een kans voor de VS om thuis serieus te gaan recyclen Duitsland zindert in recordtemperaturen in juni
Duitsland zindert in recordtemperaturen in juni Overstromingen door moesson in India meer dan 200 doden
Overstromingen door moesson in India meer dan 200 doden Degrowth is de sleutel tot het aanpakken van klimaatverandering - maar het zal niet gemakkelijk zijn
Degrowth is de sleutel tot het aanpakken van klimaatverandering - maar het zal niet gemakkelijk zijn
Hoofdlijnen
- Biologisch onderzoek suggereert dat voeding van vaders vóór seks kan bijdragen aan de gezondheid van de baby
- Een wiskundig principe legt uit hoe cellen zich met elkaar verbinden om weefsels en organen te vormen
- Was op het lichaamsoppervlak van mieren optimaliseert tegelijkertijd twee essentiële vereisten
- Veel voorkomende medicijnen tegen brandend maagzuur kunnen kanker en andere immuunstoornissen bij honden helpen bestrijden, vinden onderzoekers
- Geef de haaien niet de schuld:uit onderzoek blijkt waarom er steeds meer gehaakte tarpoenen worden gegeten
- Welk voedsel wordt geassocieerd met parasieten?
- DNA RNA en zetmeel Wat hebben deze drie belangrijke biomoleculen gemeen?
- Hergebruikt protease controleert een belangrijk signaalmolecuul-activerend eiwit
- Wat zijn twee cellen die mitose gaan ondergaan?
- Hoe langdurige blootstelling aan straling kernreactoren beschadigt

- Fasegescheiden eiwitachtige lijmen als zelforganizer van microfilamentnetwerken

- hoe vitamines, steroïden en mogelijke antivirale middelen kunnen SARS-CoV-2 beïnvloeden

- Forensische boekhouding kan toekomstige voedselfraude voorspellen

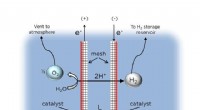
- Ingenieurs ontwikkelen drijvende boorinstallatie voor zonne-energie voor elektrolyse van zeewater
 Astronomen voeren een multifrequentie-onderzoek uit van het Melkwegachtige spiraalstelsel NGC 6744
Astronomen voeren een multifrequentie-onderzoek uit van het Melkwegachtige spiraalstelsel NGC 6744 Hoe parels precisie op nanoschaal bereiken
Hoe parels precisie op nanoschaal bereiken  Wat is plasmide en welk voordeel kan een bacterie krijgen door er een te verwerven?
Wat is plasmide en welk voordeel kan een bacterie krijgen door er een te verwerven?  Als een object tot 600 feet kan worden gegooid, wat is dan de geschatte snelheid?
Als een object tot 600 feet kan worden gegooid, wat is dan de geschatte snelheid?  Wat is het deel van de aarde dat ongeveer 3500 km dik is?
Wat is het deel van de aarde dat ongeveer 3500 km dik is?  Moleculaire dansbewegingen in slow motion vangen door witte ruis toe te voegen
Moleculaire dansbewegingen in slow motion vangen door witte ruis toe te voegen Onderzoekers maken kinetische kleding om lichaamsbewegingen te volgen
Onderzoekers maken kinetische kleding om lichaamsbewegingen te volgen Roestbescherming door nanocapsules
Roestbescherming door nanocapsules
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

