
Wetenschap
Hoeveel stikstofatomen zijn er in 7,5 g CANO32?
1. Vind de molaire massa van Ca (no₃) ₂
* Calcium (CA):40,08 g/mol
* Stikstof (N):14,01 g/mol (vermenigvuldigd met 2 omdat er twee stikstofatomen zijn)
* Zuurstof (O):16,00 g/mol (vermenigvuldigd met 6 omdat er zes zuurstofatomen zijn)
Totale molaire massa =40,08 + (14.01 * 2) + (16.00 * 6) =164.10 g/mol
2. Bereken de mol Ca (no₃) ₂
* Mol =massa / molaire massa
* Mol =7,5 g / 164,10 g / mol ≈ 0,0457 mol
3. Bereken het aantal stikstofatomen
* Elke mol van Ca (No₃) ₂ bevat 2 mol stikstofatomen.
* Totaal mol stikstofatomen =0,0457 mol * 2 =0,0914 mol
* Gebruik mol om te zetten in het aantal atomen, gebruik het nummer van Avogadro (6.022 x 10²³ Atomen/mol):
* Aantal stikstofatomen =0,0914 mol * 6.022 x 10²³ Atomen/mol ≈ 5,50 x 10²² atomen
Daarom zijn er ongeveer 5,50 x 10²² stikstofatomen in 7,5 g Ca (No₃) ₂.
 Hoe werken stralingsdetectoren?
Hoe werken stralingsdetectoren?  Waarom worden vaste stoffen in een wetenschappelijk laboratorium niet in gootstenen neergezet?
Waarom worden vaste stoffen in een wetenschappelijk laboratorium niet in gootstenen neergezet?  Overweeg de verbranding van benzine en verdamping Welk proces vertegenwoordigt een fysische verandering van chemische verandering?
Overweeg de verbranding van benzine en verdamping Welk proces vertegenwoordigt een fysische verandering van chemische verandering?  Welk type binding is ijzer(iii)chloride?
Welk type binding is ijzer(iii)chloride?  Chemische vrije kleuring van weefsel met behulp van deep learning
Chemische vrije kleuring van weefsel met behulp van deep learning
Hoofdlijnen
- Welke cellen kunnen door het menselijk oog worden gezien?
- Welke term beschrijft de theorie dat leven voortkomt uit leven?
- Wat voor soort wetenschapper bestudeert seks?
- Wat maakt mensen menselijk?
- Kunnen ziektekiemen door uw oren worden verzonden?
- Welk dier zou op het 2e trofische niveau zijn?
- Welke protist heeft een kern?
- Wat is een voorbeeld in een levend systeem van hoe moleculair van vorm is?
- De betekenis van Penta E
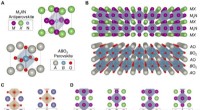
- Epitaxiale antiperovskiet/perovskiet heterostructuren voor materiaalontwerp
- Een nieuw lid in de AIE-familie
- Onderzoekers maken fotonische materialen voor krachtig, efficiënt op licht gebaseerd computergebruik

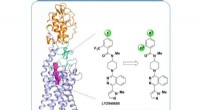
- Wetenschappers ontcijferen het multi-domein, volledige structuur van de humane smoothened receptor
- Bladaderstructuur kan de sleutel zijn tot het verlengen van de levensduur van de batterij

 Amazon betaalt slechts $ 2,2 miljoen aan belasting in het VK, ondanks stijgende winst
Amazon betaalt slechts $ 2,2 miljoen aan belasting in het VK, ondanks stijgende winst Vergelijken en contrasteren met een gematigd bioom en een Taiga Biome
Vergelijken en contrasteren met een gematigd bioom en een Taiga Biome Nieuwe planeet ontdekt in baan om jonge Melkwegster
Nieuwe planeet ontdekt in baan om jonge Melkwegster Wat is de belangrijkste functie van chromosoom?
Wat is de belangrijkste functie van chromosoom?  Onderzoekers begroeten de ondergang van een online beveiligingsalgoritme
Onderzoekers begroeten de ondergang van een online beveiligingsalgoritme Onderzoeksteam ontwerpt nieuwe poreuze materialen om onderzoek naar milieusanering te bevorderen
Onderzoeksteam ontwerpt nieuwe poreuze materialen om onderzoek naar milieusanering te bevorderen  Thermische energiewetenschapsexperimenten voor kinderen
Thermische energiewetenschapsexperimenten voor kinderen Welke rol spelen de sterren in je zonnestelsel?
Welke rol spelen de sterren in je zonnestelsel?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

