
Wetenschap
Wat is de evenwichtige vergelijking tussen natriumfosfaat en bariumacetaat?
1. Schrijf de onevenwichtige vergelijking:
Na₃po₄ (aq) + ba (ch₃coo) ₂ (aq) → ba₃ (po₄) ₂ (s) + nach₃coo (aq)
2. Breng het barium (BA) atomen in evenwicht:
2 na₃po₄ (aq) + 3 ba (ch₃coo) ₂ (aq) → ba₃ (po₄) ₂ (s) + nach₃coo (aq)
3. Breng de fosfaat (PO₄) groepen in evenwicht:
2 Na₃po₄ (aq) + 3 ba (ch₃coo) ₂ (aq) → ba₃ (po₄) ₂ (s) + 6 nach₃coo (aq)
4. Breng de natrium (NA) atomen in evenwicht:
2 Na₃po₄ (aq) + 3 ba (ch₃coo) ₂ (aq) → ba₃ (po₄) ₂ (s) + 6 nach₃coo (aq)
De gebalanceerde vergelijking is:
2 na₃po₄ (aq) + 3 ba (ch₃coo) ₂ (aq) → ba₃ (po₄) ₂ (s) + 6 nach₃coo (aq)
Verklaring:
* De reactie produceert bariumfosfaat (ba₃ (po₄) ₂ ₂ ₂ ₂ ₂ ₂ ₂ ₂ ₂ ₂ ₂ ₂ ₂ ₂ ₂ ₂ ₂ ₂ ₂ ₂ ₂ ₂ ₂ ₂ ₂ ₂ ₂ ₂ ₂ ₂ ₂ ₂) produceert, is een onoplosbare vaste stof, aangegeven door "(s)".
* Het andere product, natriumacetaat (nach₃coo), is oplosbaar en blijft in oplossing, aangegeven door "(aq)".
* De vergelijking is in evenwicht omdat er hetzelfde aantal atomen van elk element aan beide zijden van de vergelijking is.
 Sterke kunstmatige spieren van koolstofvezel kunnen 12 optillen, 600 keer hun eigen gewicht
Sterke kunstmatige spieren van koolstofvezel kunnen 12 optillen, 600 keer hun eigen gewicht Zijn moleculen rechtshandig of linkshandig? Eigenschappen van chiraal op attosecondeniveau
Zijn moleculen rechtshandig of linkshandig? Eigenschappen van chiraal op attosecondeniveau  Atomair gedispergeerd Ni is cokesbestendig voor droge reforming van methaan
Atomair gedispergeerd Ni is cokesbestendig voor droge reforming van methaan Waarom is mijnbouw van metaal slecht?
Waarom is mijnbouw van metaal slecht?  Hoeveel atomen in zinksulfide?
Hoeveel atomen in zinksulfide?
 Poplar Tree Identification
Poplar Tree Identification Wat is maatstaf voor succes in soorten Origin?
Wat is maatstaf voor succes in soorten Origin?  Wetenschappers onderzoeken verband tussen zoutgehalte van oppervlaktewater, klimaatverandering
Wetenschappers onderzoeken verband tussen zoutgehalte van oppervlaktewater, klimaatverandering Uit onderzoek blijkt dat biologisch afbreekbare theezakjes niet gemakkelijk in het milieu verslechteren
Uit onderzoek blijkt dat biologisch afbreekbare theezakjes niet gemakkelijk in het milieu verslechteren  Wat is forensische plantkunde?
Wat is forensische plantkunde?
Hoofdlijnen
- Biologen werpen licht op het mysterie van hoe microben evolueren en hun gastheren beïnvloeden
- Hoe draken werken
- Gebruik de grote ideeëncellen om variatie uit te leggen?
- Van welke vragen die leiden tot wetenschappelijke ontdekking worden geleverd?
- Hoe gebruikt plaque suiker?
- Welke chemicaliën doden gist?
- Dieren zijn geëvolueerd om overexploitatie van hun hulpbronnen te voorkomen. Kunnen mensen hetzelfde doen?
- Waarom leven fotosynthetische organismen op of nabij het oppervlak van aquatische ecosystemen?
- Waar trekt de vertaling van messenger RNA op?
- Biosensorverband verzamelt en analyseert zweet
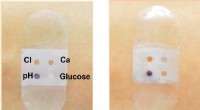
- Op weg naar autonome materialen, onderzoekers ontwerpen patronen in zelfrijdende vloeibare kristallen

- Ter zake:nieuwe kwantumsensor biedt nieuwe benadering voor vroege diagnose via beeldvorming
- Sterke M-M Pauli-afstoting leidt tot weerzinwekkende metalophiliciteit
- Zware metalen maken bodemenzymen 3 keer zwakker
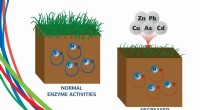
 Hoe de werkelijke kosten van energieverbruik te betalen
Hoe de werkelijke kosten van energieverbruik te betalen  Samsung plant 22 miljard dollar voor kunstmatige intelligentie auto's
Samsung plant 22 miljard dollar voor kunstmatige intelligentie auto's Wat moeten we voor het water van de aarde zorgen, dus kunnen we betekenen?
Wat moeten we voor het water van de aarde zorgen, dus kunnen we betekenen?  Hoe de natuurlijke frequentie te berekenen
Hoe de natuurlijke frequentie te berekenen Waarom warmt en koelt de oceaan langzamer op dan de atmosfeer?
Waarom warmt en koelt de oceaan langzamer op dan de atmosfeer?  Disney neemt hindernis voor samenwerking met Fox met goedkeuring van Amerikaanse toezichthouder (update)
Disney neemt hindernis voor samenwerking met Fox met goedkeuring van Amerikaanse toezichthouder (update) Kunnen koraalriffen in de toekomst spons worden?
Kunnen koraalriffen in de toekomst spons worden?  Amerikaans-Brits trio wint Nobelprijs voor geneeskunde voor ontdekking van hepatitis C
Amerikaans-Brits trio wint Nobelprijs voor geneeskunde voor ontdekking van hepatitis C
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

