
Wetenschap
Heeft zwavel een hoog of laag kookpunt?
Dit is waarom:
* Sterke intermoleculaire krachten: Zwavel bestaat als een vaste stof in zijn elementaire vorm als gevolg van sterke van der Waals -krachten tussen zijn moleculen. Deze krachten komen voort uit de grote omvang en polariseerbaarheid van zwavelatomen.
* octa-atomaire structuur: Zwavelmoleculen in hun vaste en vloeibare toestanden zijn geen enkele atomen, maar eerder acht-atoomringen (S 8 ). Deze complexe structuur draagt bij aan de hogere energie die nodig is om de bindingen te verbreken en de moleculen in staat te stellen over te gaan naar de gasvormige fase.
Het kookpunt van zwavel is 444,6 ° C (832,3 ° F). Dit is aanzienlijk hoger dan de kookpunten van veel andere elementen, zoals zuurstof (-183 ° C) of stikstof (-196 ° C), vanwege de hierboven genoemde redenen.
 Hoe ziet een grafiek van smeltpunt en bevriezende naftaleen eruit?
Hoe ziet een grafiek van smeltpunt en bevriezende naftaleen eruit?  Wat zijn drie voorbeelden voor chemische verandering?
Wat zijn drie voorbeelden voor chemische verandering?  Wat is het oxidatiegetal van dinatriumfosfaat?
Wat is het oxidatiegetal van dinatriumfosfaat?  Onderzoekers werpen licht op hoe één dodelijke ziekteverwekker zijn chemicaliën maakt
Onderzoekers werpen licht op hoe één dodelijke ziekteverwekker zijn chemicaliën maakt  Gedenatureerde alcoholversies. Isopropyl Alcohol
Gedenatureerde alcoholversies. Isopropyl Alcohol
 Oceaancirculatie is de sleutel tot het begrijpen van onzekerheden in voorspellingen van klimaatverandering
Oceaancirculatie is de sleutel tot het begrijpen van onzekerheden in voorspellingen van klimaatverandering De methaanuitstoot door de energiesector is in 2023 gestegen:IEA
De methaanuitstoot door de energiesector is in 2023 gestegen:IEA  Wat is zanderige grond?
Wat is zanderige grond?  Vorm van Lake Ontario genereert sneeuwstormen, studie toont
Vorm van Lake Ontario genereert sneeuwstormen, studie toont Is geografie een natuurwetenschap of sociale wetenschappen?
Is geografie een natuurwetenschap of sociale wetenschappen?
Hoofdlijnen
- Was Tyrannosaurus rex een roofdier of een aaseter?
- DNA-transcriptie: hoe werkt het?
- Er is dringend behoefte aan een oplossing voor een maas in de houtkap in het voorgestelde Great Koala National Park
- Wat is de rol van water voor levende organismen?
- Wat zou een arm molecule celweefsel of orgaan zijn?
- Hoe verschillen sekscellen van andere cellen in het lichaam?
- Zal klimaatverandering het risico op aflatoxine in Amerikaanse maïs vergroten?
- Wat doet microtublues?
- RNA is voor u als DNA?
- Elektrokatalysator vertoont uitstekende watersplitsingsactiviteit
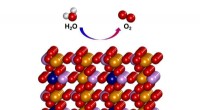
- Nieuw katalytisch proces verandert plastic zakken in lijm

- Cellen construeren levende composietpolymeren voor biomedische toepassingen
- Door schimmels geproduceerd pigment is veelbelovend als halfgeleidermateriaal

- Glas verwerken als een polymeer

 Kunstmatige intelligentie detecteert ongedierte in trailcams en volgt inheemse planten vanuit de ruimte
Kunstmatige intelligentie detecteert ongedierte in trailcams en volgt inheemse planten vanuit de ruimte Australiës krijgen een ruimteagentschap - wat nu?
Australiës krijgen een ruimteagentschap - wat nu? E-mailen tijdens Zoom-vergaderingen? Nieuw onderzoek toont de voordelen aan van multicommunicatie op het werk, in de klas
E-mailen tijdens Zoom-vergaderingen? Nieuw onderzoek toont de voordelen aan van multicommunicatie op het werk, in de klas  Welk deel beschrijft de celmembraanstructuur omdat deze flexibel is en kan worden vergeleken met een opstelling van tegels?
Welk deel beschrijft de celmembraanstructuur omdat deze flexibel is en kan worden vergeleken met een opstelling van tegels?  Vul uw benzinetank en bereid u voor om te wachten. Enkele tips om u voor te bereiden op de totale zonsverduistering van april
Vul uw benzinetank en bereid u voor om te wachten. Enkele tips om u voor te bereiden op de totale zonsverduistering van april  Klimaatverandering verandert de kustlijn van PNW nu al:stamnaties laten zien hoe ze zich kunnen aanpassen
Klimaatverandering verandert de kustlijn van PNW nu al:stamnaties laten zien hoe ze zich kunnen aanpassen  Theorie helpt bij de analyse van nucleair materiaal
Theorie helpt bij de analyse van nucleair materiaal Noem en leg het belang uit van drie wetenschappelijke gewoonten?
Noem en leg het belang uit van drie wetenschappelijke gewoonten?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

