
Wetenschap
Hoe verhoudt het aantal ionen in een zoutkristal natriumchloride zich tot chloorionen?
Dit is waarom:
* ionische binding: Natriumchloride vormt zich door ionische binding. Natriumatomen verliezen een elektron om positief geladen natriumionen (Na+) te worden. Chlooratomen krijgen een elektron om negatief geladen chloride-ionen te worden (Cl-).
* Elektrostatische aantrekkingskracht: De tegenovergestelde ladingen trekken aan en vormen een sterke elektrostatische binding.
* kristalrooster: De ionen rangschikken zichzelf in een herhalende, driedimensionale structuur die een kristalrooster wordt genoemd. Dit rooster zorgt voor een 1:1 -verhouding van natriumionen en chloride -ionen om elektrische neutraliteit te behouden.
Daarom is er voor elk natriumion in een zoutkristal één chloride -ion, waardoor ze gelijk zijn in aantal.
 Waarom worden waterstof en hydroxyl verwijderd tijdens een dehydratatiesynthesiereactie?
Waarom worden waterstof en hydroxyl verwijderd tijdens een dehydratatiesynthesiereactie?  Welk effect heeft vloeibare stikstof op moleculaire kinetische energie?
Welk effect heeft vloeibare stikstof op moleculaire kinetische energie?  Op de natuur geïnspireerde materialen kunnen worden gebruikt in toepassingen variërend van tunneling tot ruimtevaart
Op de natuur geïnspireerde materialen kunnen worden gebruikt in toepassingen variërend van tunneling tot ruimtevaart Hittebestendige enzymen zouden meer kosteneffectieve medicijnen kunnen produceren
Hittebestendige enzymen zouden meer kosteneffectieve medicijnen kunnen produceren Hydrogenering zonder waterstof:efficiënte katalyse in een stabiele emulsiegel
Hydrogenering zonder waterstof:efficiënte katalyse in een stabiele emulsiegel
 Woestijnstof uit het Midden-Oosten op het Tibetaanse plateau kan de Indiase zomermoesson beïnvloeden
Woestijnstof uit het Midden-Oosten op het Tibetaanse plateau kan de Indiase zomermoesson beïnvloeden Hoe noem je de wetenschap die gaat over de studie van het lachen?
Hoe noem je de wetenschap die gaat over de studie van het lachen?  Zorgen toeristenboten voor stress bij walvissen? Onderzoekers vinden
Zorgen toeristenboten voor stress bij walvissen? Onderzoekers vinden  Hoe wordt cederzaad verspreid?
Hoe wordt cederzaad verspreid?  Is een kever carnivore herbivoor of omnivore?
Is een kever carnivore herbivoor of omnivore?
Hoofdlijnen
- Wat is het verschil tussen cytoplasma en protoplasma?
- Welke van de volgende typen moleculen dient om te interageren met de wereld om ons heen een DNA B RNA C -eiwitten D -ribosomen?
- Welke activiteit zou de coördinatie van beide hersenen van de hemisferen vereisen?
- Wat laat mitose organismen toe?
- Wat omvat de beweging van materialen in cel en tussen onderdelen een meerachtig organisme?
- Is het waar dat DNA -replicatie ook mitose kan worden genoemd?
- Welke organismen eten olie?
- Waar codeert een groep van drie nucleotiden voor?
- Wat is de term voor het vermogen van een organisme om te overleven en zich voort te planten?
- Cohesieonderzoekers ontrafelen het mysterie van waterstofeffecten op materialen

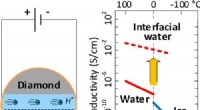
- Wetenschappers meten de elektrische geleidbaarheid van zuiver grensvlakwater
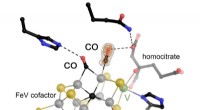
- Vanadiumafhankelijke stikstofase kan twee CO-moleculen tegelijk binden
- Ingenieurs maken slimme aerogel die lucht in drinkwater verandert

- Chemici synthetiseren moleculaire pretzels
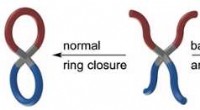
 Autofabrikanten kiezen voor Trump in juridisch gevecht met Californië
Autofabrikanten kiezen voor Trump in juridisch gevecht met Californië Digitale mapping van het spoornetwerk levert efficiëntiewinst op
Digitale mapping van het spoornetwerk levert efficiëntiewinst op Wat is de relatie tussen structuur van een atoom- en atoomspectra?
Wat is de relatie tussen structuur van een atoom- en atoomspectra?  NASA-nachtbeeld toont orkaan Paulettes met grote ogen naderen Bermuda
NASA-nachtbeeld toont orkaan Paulettes met grote ogen naderen Bermuda Wat is de minimale hoeveelheid valentie -elektronen die een atoom kan hebben?
Wat is de minimale hoeveelheid valentie -elektronen die een atoom kan hebben?  Zorgen over hoofdletsel politie
Zorgen over hoofdletsel politie Nieuwe cycloonvoorspellingen:waarom gevolgen de focus zouden moeten zijn van waarschuwingen voor gevaarlijk weer
Nieuwe cycloonvoorspellingen:waarom gevolgen de focus zouden moeten zijn van waarschuwingen voor gevaarlijk weer  Wat is 97,5 graden Fahrenheit in Celsius?
Wat is 97,5 graden Fahrenheit in Celsius?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

