
Wetenschap
Waarom is het vermogen van het caten het hoogst voor koolstofatomen?
1. Kleine atoommaat: Koolstofatomen zijn relatief klein, waardoor ze sterke covalente bindingen met elkaar kunnen vormen. Deze strakke binding is essentieel voor het vormen van lange ketens.
2. Sterke C-C-binding: Koolstof vormt zeer sterke, dubbele en drievoudige bindingen met zichzelf. Deze sterkte draagt bij aan de stabiliteit van lange koolstofketens.
3. Tetravalentie: Koolstof heeft vier valentie -elektronen, waardoor het vier covalente bindingen kan vormen. Dit zorgt voor vertakking en complexe driedimensionale structuren.
4. Mogelijkheid om stabiele bindingen te vormen met andere elementen: Koolstof kan sterke bindingen vormen met waterstof, zuurstof, stikstof en andere elementen, wat leidt tot een grote verscheidenheid aan organische verbindingen.
5. Gebrek aan D-orbitalen: In tegenstelling tot zwaardere elementen in dezelfde groep, heeft koolstof geen beschikbare D-orbitalen. Dit voorkomt de vorming van meer dan vier bindingen, wat bijdraagt aan de stabiliteit van koolstofketens.
Vergelijking met andere elementen:
* silicium: Silicium, hoewel ook in groep 14, heeft zwakkere Si-Si-bindingen en grotere atoomgrootte, waardoor het minder vatbaar is voor catenatie.
* Andere elementen: Andere elementen, zoals zuurstof, stikstof en fosfor, hebben beperkte casteningsmogelijkheden vanwege hun neiging om meerdere bindingen met zichzelf te vormen, wat leidt tot onstabiele kettingstructuren.
Samenvattend:
De combinatie van kleine, sterke C-C-bindingen, tetravalentie en het ontbreken van D-orbitalen maakt koolstof uniek geschikt voor het vormen van lange, stabiele ketens en complexe structuren, waardoor het het hoogste kattenvermogen krijgt bij alle elementen. Dit vermogen is de basis van organische chemie en de diverse wereld van op koolstof gebaseerde moleculen.
 Zijn de eigenschappen van een verbinding doorgaans dezelfde als die van de elementen waaruit deze is gemaakt?
Zijn de eigenschappen van een verbinding doorgaans dezelfde als die van de elementen waaruit deze is gemaakt?  Wat gebeurt er met het volume vloeistoffen en gassen van vaste stoffen als ze cool zijn?
Wat gebeurt er met het volume vloeistoffen en gassen van vaste stoffen als ze cool zijn?  Hoe benzine werkt
Hoe benzine werkt  Onderzoekers ontdekken hoe de natuur ammoniumtransporteurs hergebruikt als receptoren
Onderzoekers ontdekken hoe de natuur ammoniumtransporteurs hergebruikt als receptoren  Kalium geeft op perovskiet gebaseerde zonnecellen een efficiëntieboost
Kalium geeft op perovskiet gebaseerde zonnecellen een efficiëntieboost
 Hoe Brazilië de kansen kan verslaan en een enorm deel van de Amazone kan herstellen
Hoe Brazilië de kansen kan verslaan en een enorm deel van de Amazone kan herstellen Onderzoek wijst uit dat schade door overstromingen aan dijken cumulatief is - en vaak onzichtbaar
Onderzoek wijst uit dat schade door overstromingen aan dijken cumulatief is - en vaak onzichtbaar Onderzoekers gebruiken GPS om te ontdekken hoe mensen nationale parken gebruiken
Onderzoekers gebruiken GPS om te ontdekken hoe mensen nationale parken gebruiken  Wetenschappers onthullen effecten van water op 660 km discontinuïteit in de diepe aarde
Wetenschappers onthullen effecten van water op 660 km discontinuïteit in de diepe aarde NASA-onderzoek naar droogte toont de waarde van klimaatmitigatie aan, aanpassing
NASA-onderzoek naar droogte toont de waarde van klimaatmitigatie aan, aanpassing
Hoofdlijnen
- Wanneer het menselijk lichaam zijn verdediging tegen een ziekteverwekkers mobiliseert, herkent pathogenen?
- Welke celstructuur dient als grens ten opzichte van zijn omgeving?
- Wat doen vertakkende cellen?
- Biologen bestuderen de afwegingen tussen microscopische roofdieren
- Wat is de stapel membranen in chloroplast?
- Big data-algoritmen kunnen discrimineren, en het is niet duidelijk wat we daaraan moeten doen
- Waarom ramon y Cajal neuronen de vlinder naar ziel genoemd?
- Welk hormoon produceert de pancrease?
- Wat zijn de fasen in fytomining?
- Onderzoekers ontwerpen een op nanotechnologie gebaseerd systeem dat methaan kan transporteren met lagere druk en lagere kosten
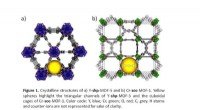
- Het delen van gegevens is de toekomst van materiaalonderzoek

- Onderzoekers passen E. coli aan om planten om te zetten in hernieuwbare chemicaliën

- Het regent diamanten in het universum, suggereert onderzoek

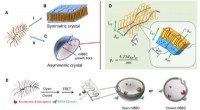
- De kristalsymmetrie van de natuur onderbreken om gerichte medicijnafgifte te bevorderen
 Japans bedrijf plant kunstmatige meteorenregen
Japans bedrijf plant kunstmatige meteorenregen Zeer rekbare vezelvormige supercondensator op basis van koolstofnanobuisjes
Zeer rekbare vezelvormige supercondensator op basis van koolstofnanobuisjes Is een Hertz elke seconde of minuut vibratie?
Is een Hertz elke seconde of minuut vibratie?  Wat is de lengte van een asteroïde?
Wat is de lengte van een asteroïde?  Wetenschappers onthullen oorzaken van langdurige lente-zomerdroogte boven Noord-China
Wetenschappers onthullen oorzaken van langdurige lente-zomerdroogte boven Noord-China Hoeveel is 2 gram in kg?
Hoeveel is 2 gram in kg?  Hoe de zoekmachine van LinkedIn een gendervooroordeel kan weerspiegelen
Hoe de zoekmachine van LinkedIn een gendervooroordeel kan weerspiegelen  Quick & Easy Science Fair Projects voor 8e Graders
Quick & Easy Science Fair Projects voor 8e Graders
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

