
Wetenschap
Atomen van hetzelfde element met verschillende atoommassa's?
Hier is een uitsplitsing:
* element: Een stof die bestaat uit slechts één type atoom. Koolstof is bijvoorbeeld een element.
* Atomische massa: De massa van een atoom, voornamelijk bepaald door het aantal protonen en neutronen in zijn kern.
* isotopen: Atomen van hetzelfde element die hetzelfde aantal protonen hebben (en dus hetzelfde atoomnummer) maar verschillen in het aantal neutronen. Dit betekent dat ze verschillende atoommassa's hebben.
Voorbeeld:
* carbon-12: Heeft 6 protonen en 6 neutronen (atomaire massa =12)
* carbon-14: Heeft 6 protonen en 8 neutronen (atomaire massa =14)
Zowel carbon-12 als koolstof-14 zijn isotopen van koolstof omdat ze allebei 6 protonen hebben, maar ze verschillen in hun neutronentelling, wat resulteert in verschillende atoommassa's.
Belangrijke punten over isotopen:
* Dezelfde chemische eigenschappen: Isotopen van hetzelfde element hebben over het algemeen dezelfde chemische eigenschappen omdat ze hetzelfde aantal elektronen hebben, die chemische binding bepalen.
* Verschillende fysische eigenschappen: Isotopen kunnen iets verschillende fysieke eigenschappen hebben, zoals dichtheid of smeltpunt.
* Radioactieve isotopen: Sommige isotopen zijn radioactief, wat betekent dat hun kernen in de loop van de tijd onstabiel en verval zijn.
Het begrijpen van isotopen is cruciaal op veel gebieden, waaronder:
* chemie: Radioactieve isotopen worden gebruikt bij dating en het traceren van chemische reacties.
* geneeskunde: Radioactieve isotopen worden gebruikt bij medische beeldvorming en behandeling.
* Geologie: Radioactieve isotopen worden gebruikt tot datum rotsen en fossielen.
 Mushroom Hunting in Georgia
Mushroom Hunting in Georgia De luchtkwaliteit in de VS neemt af na jaren van verbetering
De luchtkwaliteit in de VS neemt af na jaren van verbetering Uit onderzoek blijkt dat het brandstofverbruik van een auto kan worden geannuleerd bij uw volgende aankoop van een auto
Uit onderzoek blijkt dat het brandstofverbruik van een auto kan worden geannuleerd bij uw volgende aankoop van een auto Science Concepts for Kids
Science Concepts for Kids  De hitte is aan:wat we weten over waarom de oceaantemperaturen records blijven breken
De hitte is aan:wat we weten over waarom de oceaantemperaturen records blijven breken
Hoofdlijnen
- Hoe is de bevruchting anders dan de ontwikkeling van het embryo?
- Wat betekent forsts in de wetenschap?
- Hoe voorkom je virusuitbraken? Door de diergezondheid te beschermen
- Hoe verschillen de reproductieve structuren van een typisch-gymnosperm van elkaar?
- Wat is met plant geassocieerde schimmels?
- De hoge en machtige Himalaya:een broeinest van biodiversiteit die voor grote uitdagingen staat
- Wat zijn verschillende functies van wortels in planten?
- Wat is het verschil tussen veterinaire bioscience en dierenbioscience?
- Welke is kleinere zetmeelkorrel of tracheale cel?
- Onderzoekers gebruiken Theta voor realtime analyse van COVID-19-eiwitten
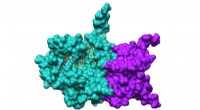
- Computermodellering van WNK-kinaseremmers kan nieuwe hulpmiddelen bieden voor het begrijpen van hypertensie
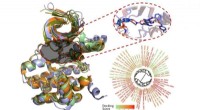
- Nieuw polymeer verbetert het vermogen van tribo-elektrische nanogeneratoren

- Gecontroleerde faagtherapie kan zich richten op medicijnresistente bacteriën en tegelijkertijd mogelijke onbedoelde gevolgen omzeilen

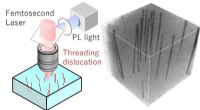
- Niet-destructieve karakteriseringstechniek helpt bij de ontwikkeling van galliumnitridekristallen
 Weer op Mars:kil met kans op stofduivels
Weer op Mars:kil met kans op stofduivels Hoe noemen we de chemische stof die cellen nodig hebben om te werken en te reproduceren?
Hoe noemen we de chemische stof die cellen nodig hebben om te werken en te reproduceren?  Welk item is gemaakt door mensen die de middelen van fysische en chemische verwering kunnen worden afgebroken?
Welk item is gemaakt door mensen die de middelen van fysische en chemische verwering kunnen worden afgebroken?  Openbaar internaat:de manier om onderwijsproblemen op te lossen?
Openbaar internaat:de manier om onderwijsproblemen op te lossen?  Wat gebeurt er als de maan zou worden vervangen voor een object met een massa Jupiter?
Wat gebeurt er als de maan zou worden vervangen voor een object met een massa Jupiter?  Oplosmiddeleffect op filmvorming en apparaatprestaties voor 2D Dion-Jacobson perovskiet-zonnecellen
Oplosmiddeleffect op filmvorming en apparaatprestaties voor 2D Dion-Jacobson perovskiet-zonnecellen  Geactiveerd grafeen maakt superieure supercondensatoren voor energieopslag
Geactiveerd grafeen maakt superieure supercondensatoren voor energieopslag Wat is topografie?
Wat is topografie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

