
Wetenschap
Waarom verandert de kleur met sulfaat?
Dit is waarom:
* sulfaationen zijn kleurloos: Ze absorberen of stoten niet zichtbaar licht uit, daarom hebben ze geen eigen kleur.
* kleurveranderingen zijn te wijten aan andere verbindingen: Als u een kleurverandering ziet in een oplossing die sulfaationen bevat, is dit waarschijnlijk vanwege een chemische reactie waarbij andere stoffen in de oplossing betrokken zijn. Bijvoorbeeld:
* Vorming van een gekleurd neerslag: Als een metaalkation reageert met sulfaationen, kan deze een onoplosbare vaste stof (neerslag) vormen met een kleur. Bariumsulfaat (Baso₄) is bijvoorbeeld een wit neerslag.
* Redox -reacties: Sommige reacties met sulfaationen kunnen een verandering in oxidatietoestanden van andere elementen met zich meebrengen, wat leidt tot een kleurverandering. De reductie van chromaationen (Cro₄²⁻) tot chromietionen (cr³⁺) in aanwezigheid van sulfaationen kan bijvoorbeeld resulteren in een kleurverandering van geel naar groen.
Kortom, sulfaationen zelf veranderen niet van kleur. Het zijn de andere stoffen die aanwezig zijn in de oplossing en de reacties die ze ondergaan die leiden tot kleurveranderingen.
 Hoe krijg je schonere lucht? Duitsland overweegt gratis openbaar vervoer
Hoe krijg je schonere lucht? Duitsland overweegt gratis openbaar vervoer Oproep voor ingenieurs om op te treden tegen klimaatverandering
Oproep voor ingenieurs om op te treden tegen klimaatverandering EPA-regel om gassen in koelkasten uit te faseren, koelvloeistoffen
EPA-regel om gassen in koelkasten uit te faseren, koelvloeistoffen Lijst van insecten met onvolledige metamorfose
Lijst van insecten met onvolledige metamorfose Nieuw onderzoek in de VS en Europa laat zien hoe invasieve plantensoorten het beter doen dan inheemse plantensoorten
Nieuw onderzoek in de VS en Europa laat zien hoe invasieve plantensoorten het beter doen dan inheemse plantensoorten
Hoofdlijnen
- Wanneer is de beste tijd van de dag om een beslissing te nemen?
- Wat vormen diatomeeën zich meestal?
- Hoe de kern vormt een pollenkorrel die een vrouwelijke eiercel bemoeilijkt?
- Wat zijn de DNA -moleculen gevonden in celorganel?
- Doorbreken van peulvruchten gewas wilde relatieve barrière
- Structuren die uit het lichaam groeien, worden genoemd?
- Een organisme heeft een haploïd nummer van 36. Wat is het diploïde nummer?
- Het boodschapper-RNA doden -- Maar welke?
- Welke oranismen hebben de meeste kenmerken gemeen met leden van een soort of leden van een orde?
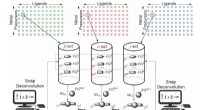
- Een manier om het ontdekken van reacties te versnellen met behulp van automatisering
- Ammoniak:een troef voor het energietransitieproces

- Groenere waterstof uit water

- Onderzoekers ontwikkelen een niet-invasieve test voor rookverontreiniging in wijngaarden

- Wetenschappers demonstreren de eerste chemisch gesynthetiseerde optische schakelaar

 Is het aantal elektronen in de kern van een atoom dat atoomnummer?
Is het aantal elektronen in de kern van een atoom dat atoomnummer?  Hoe zijn atomen in de binnenkant?
Hoe zijn atomen in de binnenkant?  Hoe maakt opvolging een vijver in het bos?
Hoe maakt opvolging een vijver in het bos?  Huidkankermysterie onthuld in yin- en yang-eiwit
Huidkankermysterie onthuld in yin- en yang-eiwit Wat werd ontdekt toen Apollo 11 naar de maan ging?
Wat werd ontdekt toen Apollo 11 naar de maan ging?  Wereldwijde studie onthult groot vastgesteld netto risico voor zeldzame, gekoesterde NZ pinguïn
Wereldwijde studie onthult groot vastgesteld netto risico voor zeldzame, gekoesterde NZ pinguïn Welke caracteristieken van de zon zouden het een moeilijke plek maken om te verkennen of te bezoeken?
Welke caracteristieken van de zon zouden het een moeilijke plek maken om te verkennen of te bezoeken?  Wat is Nemesis?
Wat is Nemesis?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

