
Wetenschap
Bij de volledige verbranding van C3H8O3 hoeveel koolstofdioxide wordt er geproduceerd wanneer 23,0 g brandwonden?
1. Schrijf de gebalanceerde chemische vergelijking:
C₃h₈o₃ + 4 o₂ → 3 co₂ + 4 h₂o
Deze vergelijking vertelt ons dat voor elke mol van C₃h₈o₃ die brandt, 3 mol co₂ worden geproduceerd.
2. Bereken de molaire massa van C₃h₈o₃:
* C:12.01 g/mol * 3 =36,03 g/mol
* H:1.01 g/mol * 8 =8,08 g/mol
* O:16.00 g/mol * 3 =48,00 g/mol
* Totale molaire massa:36.03 + 8.08 + 48.00 =92.11 g/mol
3. Converteer gram van c₃h₈o₃ in mol:
* Moles =gram / molaire massa
* Mol =23,0 g / 92.11 g / mol =0,250 mol C₃h₈o₃
4. Gebruik de molverhouding van de gebalanceerde vergelijking om mol Co₂ te vinden:
* Uit de vergelijking:1 mol C₃h₈o₃ produceert 3 mol co₂
* Mol Co₂ =0,250 mol C₃h₈o₃ * (3 mol co₂ / 1 mol C₃h₈o₃) =0.750 mol Co₂
Daarom worden 0,750 mol kooldioxide geproduceerd wanneer 23,0 g C₃h₈o₃ brandwonden.
 'S Werelds meest efficiënte productie van succinaat uit koolstofdioxide
'S Werelds meest efficiënte productie van succinaat uit koolstofdioxide Waarom komen verbindingen van XE vaker voor in vergelijking met andere edelgassen?
Waarom komen verbindingen van XE vaker voor in vergelijking met andere edelgassen?  Eigenschappen van Heat Absorption van Salt
Eigenschappen van Heat Absorption van Salt ArtSea Ink:een kleurrijke, Op zeewier gebaseerde inkt voor 3D-printen
ArtSea Ink:een kleurrijke, Op zeewier gebaseerde inkt voor 3D-printen Wat zijn enkele veel voorkomende huishoudelijke zuren en basen?
Wat zijn enkele veel voorkomende huishoudelijke zuren en basen?
 Bittere kou in januari zal het ongedierte in de veldgewassen waarschijnlijk niet verminderen
Bittere kou in januari zal het ongedierte in de veldgewassen waarschijnlijk niet verminderen Een dessertachtige woestijn:Californische lithosfeer lijkt op crème brûlée
Een dessertachtige woestijn:Californische lithosfeer lijkt op crème brûlée Mars-wetenschappers onderzoeken het oude leven in Australië
Mars-wetenschappers onderzoeken het oude leven in Australië Australië ontwikkelt satelliet om gevarenzones voor bosbranden te voorspellen
Australië ontwikkelt satelliet om gevarenzones voor bosbranden te voorspellen Wat houdt stof op zijn plaats?
Wat houdt stof op zijn plaats?
Hoofdlijnen
- Hoeveel aminozuren worden geproduceerd door het DNA -segment dat 21 basen heeft?
- Wat doen wetenschappers na een onderzoek?
- Wetenschappelijke benadering heeft zijn intellectuele wortel in?
- Hoe is de breedste categorie in de biologische taxonomie?
- Heeft volwassen rode bloedcellen chromosomen?
- Wat betekent echt verschil in de wetenschap?
- Hebben onderzoekers de ontbrekende schakel gevonden die eenvoudige eiwitsequencing mogelijk maakt?
- Hoe is marshmallow gerelateerd aan colloïdale systemen?
- Wat gebeurt er op een microscopisch niveau tijdens homeostase?
- Niet zo fantastisch plastic voor eenmalig gebruik om een milieuvriendelijke make-over te krijgen

- Regelen van de eigenschappen van een eenkristal via spanning en toepassing

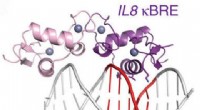
- Duel van de inflammatoire hoofdregulatoren - inzichten voor het ontdekken van medicijnen
- Onderzoekers gebruiken kunstmatige neurale netwerken om het testen van materialen te stroomlijnen

- Zilver verbetert de efficiëntie van monograinlaagzonnecellen

 Wat is geen uitkomst van de omgeving die een fenotype wijzigt?
Wat is geen uitkomst van de omgeving die een fenotype wijzigt?  Wat is de definitie van gen?
Wat is de definitie van gen?  Uitzoeken hoe je de regoliet van de maan kunt inademen
Uitzoeken hoe je de regoliet van de maan kunt inademen  Experts:Amerikaanse anti-Huawei-campagne waarschijnlijk overdreven
Experts:Amerikaanse anti-Huawei-campagne waarschijnlijk overdreven Vergulde kristallen zetten nieuwe standaard voor aardgasdetectoren
Vergulde kristallen zetten nieuwe standaard voor aardgasdetectoren Hoe dans studenten in STEM-disciplines kan helpen
Hoe dans studenten in STEM-disciplines kan helpen Is geologie een wetenschap of sociale wetenschappen?
Is geologie een wetenschap of sociale wetenschappen?  Californias Paradise:een spookstad die uit de hel komt
Californias Paradise:een spookstad die uit de hel komt
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

