
Wetenschap
Wat vertelt u hoeveel atomen of moleculen van een reactant -product deelnemen aan reactie?
Hier is hoe het werkt:
* Balanced chemische vergelijking: Een chemische vergelijking is in balans wanneer het aantal atomen van elk element aan de reactantzijde (links) gelijk is aan het aantal atomen van dat element aan de productzijde (rechts). Dit zorgt ervoor dat massa wordt behouden tijdens de reactie.
* stoichiometrische coëfficiënten: Dit zijn de getallen geschreven voor elke chemische formule in een evenwichtige vergelijking. Ze vertegenwoordigen het relatieve aantal mol (en dus atomen of moleculen) van elke stof die bij de reactie betrokken is.
Voorbeeld:
De evenwichtige chemische vergelijking voor de verbranding van methaan is:
`` `
Ch₄ + 2o₂ → co₂ + 2h₂o
`` `
* reactanten: Methaan (ch₄) en zuurstof (o₂)
* Producten: Koolstofdioxide (CO₂) en water (H₂o)
Interpretatie:
* 1 molecuul van methaan reageert met 2 moleculen van zuurstof.
* Dit produceert 1 molecuul van koolstofdioxide en 2 moleculen van water.
Sleutelpunten:
* Stoichiometrische coëfficiënten zijn cruciaal voor het begrijpen van de kwantitatieve relaties in chemische reacties.
* Hiermee kunt u de hoeveelheid product gevormd uit een bepaalde hoeveelheid reactant of vice versa voorspellen.
* Het is belangrijk om te onthouden dat coëfficiënten mol vertegenwoordigen, geen individuele moleculen of atomen.
Laat het me weten als je nog meer vragen hebt!
 Welke zou sneller ijs smelten in een pot met water of kuip warm water?
Welke zou sneller ijs smelten in een pot met water of kuip warm water?  Zwak zuur of basis waarvan de kleur afhankelijk is van de concentratie van hydroniumionen?
Zwak zuur of basis waarvan de kleur afhankelijk is van de concentratie van hydroniumionen?  Wat is het aantal atomen in H2SO4?
Wat is het aantal atomen in H2SO4?  Welk type binding vormt een vetzuur voor 3-koolstofbackbone?
Welk type binding vormt een vetzuur voor 3-koolstofbackbone?  Wat zijn enkele fysieke verschillen tussen de twee belangrijkste allotropen van zuurstof?
Wat zijn enkele fysieke verschillen tussen de twee belangrijkste allotropen van zuurstof?
Hoofdlijnen
- Wat zijn de stadia van biologische verwering?
- Wat is het type wetenschap met voorlopige explantatie?
- Onderzoek laat zien hoe ribosomen hun blokkades opheffen
- Hoe vindt ranciditeit plaats?
- Is een zonnebloem prokaryotisch of eukaryotisch?
- Wat is de volgorde van base os agctcag op tegenover Strand?
- Waarom is het proces van hemiosmose belangrijk voor mensen?
- Wat zijn de purine basen van DNA?
- Is de term cerebrale dominantie het halfrond aan dat dominant is voor taal?
- Afval van het maken van paarse maïschips levert een natuurlijke kleurstof op, supplementen, kattenbakvulling

- Op hydrogel gebaseerde elektroden voor hersenimplantaten ontwikkeld

- Infraroodsensor dient als een nieuw hulpmiddel voor het ontdekken van medicijnen

- Gras vervangt plastic in meeneemverpakkingen

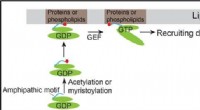
- Onderzoekers ontdekken een nieuw mechanisme voor het werven van ARF-familie-eiwitten
 Is de Hubble -telescoop helemaal in de exosfeer of buiten de atmosfeer?
Is de Hubble -telescoop helemaal in de exosfeer of buiten de atmosfeer?  Onderzoekers ontwikkelen fotoactiveerbare nanogeneeskunde voor de behandeling van leeftijdsgebonden maculaire degeneratie
Onderzoekers ontwikkelen fotoactiveerbare nanogeneeskunde voor de behandeling van leeftijdsgebonden maculaire degeneratie  Waarom hebben vloeistoffen een vast volume maar geen vorm?
Waarom hebben vloeistoffen een vast volume maar geen vorm?  Indringende vraag:Worden kunstenaars geboren of onderwezen?
Indringende vraag:Worden kunstenaars geboren of onderwezen?  Welke organismen eten nereis?
Welke organismen eten nereis?  Een zonne-uitbarsting volgen door het zonnestelsel
Een zonne-uitbarsting volgen door het zonnestelsel Hoe maak je een krachtige DC elektromagneet
Hoe maak je een krachtige DC elektromagneet  Is Google na het onderzoek van Facebook de volgende?
Is Google na het onderzoek van Facebook de volgende?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

