
Wetenschap
Wat is waar aan de elementen fluorchloor en jodium?
* het zijn allemaal halogenen. Dit betekent dat ze behoren tot groep 17 (VIIA) van het periodiek systeem.
* het zijn allemaal niet -metalen. Ze hebben de neiging om elektronen te verwerven om negatieve ionen te vormen.
* ze zijn allemaal zeer reactief. Dit komt omdat ze zeven valentie -elektronen hebben en sterk willen om er nog een te winnen om een stabiel octet te bereiken.
* hun reactiviteit vermindert de groep af. Fluor is het meest reactief, gevolgd door chloor, vervolgens broom en uiteindelijk jodium. Dit komt door de toenemende atoomgrootte en het afnemende elektronegativiteit terwijl u de groep doorgaat.
* Ze worden allemaal in de natuur gevonden als diatomaire moleculen. Dit betekent dat ze bestaan als paren van atomen aan elkaar zijn gebonden (F2, CL2, I2).
* Het zijn allemaal essentiële elementen. Ze zijn belangrijk voor verschillende biologische processen en spelen cruciale rollen in het menselijk lichaam. Chloor is bijvoorbeeld cruciaal voor het handhaven van de juiste hydratatie en elektrolytbalans, terwijl jodium essentieel is voor de productie van schildklierhormoon.
Belangrijke opmerking: Hoewel deze elementen essentieel zijn, zijn ze ook zeer reactief en potentieel gevaarlijk in hun elementaire vormen.
 Verhoogt het verwijderen van waterstof de zuurgraad?
Verhoogt het verwijderen van waterstof de zuurgraad?  Enzym die de chemische afbraak van een stof veroorzaakt?
Enzym die de chemische afbraak van een stof veroorzaakt?  Hoog-entropie-gestabiliseerde chalcogeniden met hoge thermo-elektrische prestaties
Hoog-entropie-gestabiliseerde chalcogeniden met hoge thermo-elektrische prestaties Welk zuur is een sterke elektrolyt A. zwavelzuur B. azijnzuur C. mierenzuur D. citroenzuur?
Welk zuur is een sterke elektrolyt A. zwavelzuur B. azijnzuur C. mierenzuur D. citroenzuur?  Als je van een gas naar vaste stof gaat, is het endotherm?
Als je van een gas naar vaste stof gaat, is het endotherm?
 Is het waarschijnlijker dat op technologie gebaseerde intelligentie zich op het land of in het water zal ontwikkelen?
Is het waarschijnlijker dat op technologie gebaseerde intelligentie zich op het land of in het water zal ontwikkelen?  De kust van Louisiana heeft nog steeds last van stormen, zich schrap zetten voor meer
De kust van Louisiana heeft nog steeds last van stormen, zich schrap zetten voor meer Onderzoekers stellen een regeling voor die koolstofemissies behandelt als financiële schulden
Onderzoekers stellen een regeling voor die koolstofemissies behandelt als financiële schulden Onderzoekers gebruiken met succes gedistribueerde akoestische detectie voor seismische monitoring
Onderzoekers gebruiken met succes gedistribueerde akoestische detectie voor seismische monitoring Expert onderzoekt de afwegingen waarmee bedrijven worden geconfronteerd wanneer ze worstelen met duurzaamheidskwesties
Expert onderzoekt de afwegingen waarmee bedrijven worden geconfronteerd wanneer ze worstelen met duurzaamheidskwesties
Hoofdlijnen
- Beschrijf het pad van elektronen uit de tijd dat ze intermembraanruimte in mitochondrion binnenkomen om te worden geretourneerd in Mitochondrion?
- Wat is het eerste woord in taxonomie?
- Waarom de wetenschap niet helpt bij het verkopen van chocoladekoekjes
- Wat is de wijze van reproductie ongemeenlijk?
- Hoe planten microben benutten om voedingsstoffen binnen te krijgen
- Hoe ondersteunt genetica de evolutie?
- Hoe helpt klimaatverandering ziekten te verspreiden?
- Hebben plant en schimmels beide een kern?
- Wat is de mythe van Callisto?
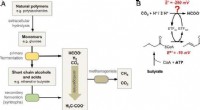
- Cruciale stap geïdentificeerd in de omzetting van biomassa naar methaan
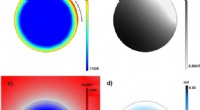
- Ontwikkeling van een 3D-deeltjesmodel voor afzonderlijke deeltjes in batterij-elektroden
- Waterstof:brandstof van de toekomst?

- Simulaties laten zien hoe bèta-amyloïde neurale cellen kan doden

- Inzichten in het gedrag van constructiematerialen in een omgeving met gesmolten zout

 Cyberbeveiliging vereist internationale samenwerking, vertrouwen
Cyberbeveiliging vereist internationale samenwerking, vertrouwen Waarom beweegt een object sneller op een recht pad dan gebogen pad?
Waarom beweegt een object sneller op een recht pad dan gebogen pad?  Statistische modellering helpt visserijbeheerders invasieve soorten te verwijderen
Statistische modellering helpt visserijbeheerders invasieve soorten te verwijderen Wat is de naam Super Giant in Orion?
Wat is de naam Super Giant in Orion?  Feiten over Colorado State voor Kids
Feiten over Colorado State voor Kids Wat is de rol RNA tijdens vertaling?
Wat is de rol RNA tijdens vertaling?  Hoe breken Linnaeus organismen in groepen-de groepen waren gebaseerd op wat?
Hoe breken Linnaeus organismen in groepen-de groepen waren gebaseerd op wat?  Wat is de volledige redoxreactie voor MNO4- en H2O2 onder zure omstandigheden?
Wat is de volledige redoxreactie voor MNO4- en H2O2 onder zure omstandigheden?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

