
Wetenschap
Vergelijk de kook- en vriespunten van 1M -oplossing glucose met een CACL2. Waarom heeft CACL2 een hogere lager, leg het niet alleen uit, zeg dan dat het dan 3M is?
Kookpunthoogte
* Glucose: Een glucose -oplossing van 1 m zal een iets hoger kookpunt hebben dan zuiver water.
* CACL2: Een 1M CACL2 -oplossing zal een aanzienlijk hoger kookpunt hebben dan zuiver water.
Point Point Depression
* Glucose: Een glucose -oplossing van 1 m zal een iets lager vriespunt hebben dan zuiver water.
* CACL2: Een 1M CACL2 -oplossing zal een aanzienlijk lager vriespunt hebben dan zuiver water.
Waarom het verschil?
Het verschil in kookpunthoogte en vriespuntdepressie komt voort uit het concept van colligatieve eigenschappen . Colligatieve eigenschappen hangen uitsluitend af van het aantal opgeloste deeltjes in een oplossing, niet van het type deeltjes.
Hier is hoe het werkt:
* dissociatie: Glucose is een moleculaire verbinding en dissocieert niet in ionen wanneer opgelost in water. Het blijft als individuele glucosemoleculen.
* ionisatie: CACL2 is een ionische verbinding en dissocieert in ionen wanneer opgelost in water. Eén formule -eenheid van CACL2 produceert drie ionen:één ca²⁺ ion en twee cl⁻ -ionen.
De impact van ionen:
* meer deeltjes: De ionisatie van CACL2 betekent dat een oplossing van 1 m daadwerkelijk drie keer bevat het aantal deeltjes als een glucose -oplossing van 1 m. Deze hogere concentratie deeltjes heeft een groter effect op de colligatieve eigenschappen.
* verstoring van de oplosmiddelstructuur: De ionen van CACL2 verstoren het waterstofbindingsnetwerk van watermoleculen, waardoor het moeilijker is om een vaste structuur te vormen (bevriezen) en het voor hen gemakkelijker te ontsnappen in de dampfase (koken).
Samenvattend
Hoewel zowel glucose- als CACL2 -oplossingen kookpunthoogte en vriespuntdepressie vertonen, is de grootte van deze effecten veel groter voor CACL2 omdat het meer deeltjes in oplossing produceert als gevolg van ionisatie. Dit is een direct gevolg van de colligatieve eigenschappen van oplossingen.
 Wat zijn enkele toepassingen voor zwavel in de niet-voedings- of dranksector?
Wat zijn enkele toepassingen voor zwavel in de niet-voedings- of dranksector?  Waarom zou je een tang gebruiken om met natrium om te gaan?
Waarom zou je een tang gebruiken om met natrium om te gaan?  Welke is warmer 1C of 69F?
Welke is warmer 1C of 69F?  Een wetenschapper voerde een experiment uit om te bepalen hoe zuren een nieuw ontdekt metaal beïnvloeden, was zorgvuldig de stappen van haar, evenals observaties en resultaten?
Een wetenschapper voerde een experiment uit om te bepalen hoe zuren een nieuw ontdekt metaal beïnvloeden, was zorgvuldig de stappen van haar, evenals observaties en resultaten?  Hoeveel moleculen van H2O is gelijk aan 1 mol H2O?
Hoeveel moleculen van H2O is gelijk aan 1 mol H2O?
 Waarom is de interne structuur van de aarde belangrijk?
Waarom is de interne structuur van de aarde belangrijk?  Fransman probeert Atlantische Oceaan over te steken in vatcapsule
Fransman probeert Atlantische Oceaan over te steken in vatcapsule wereldwijd, overstromingen lijken af te nemen, zelfs als extreme regenval toeneemt. Waarom?
wereldwijd, overstromingen lijken af te nemen, zelfs als extreme regenval toeneemt. Waarom? Hoe lezen paarden menselijke emotionele signalen?
Hoe lezen paarden menselijke emotionele signalen?  De effecten van menselijke interventie op het milieu
De effecten van menselijke interventie op het milieu
Hoofdlijnen
- Tot welke tak van de wetenschap is pasteurisatie?
- Een protist die zijn eigen voedsel maakt, is een?
- Telt de menselijke mond als orgaan?
- Welke van de volgende paden produceert de meeste NADH en de minste ATP?
- Wordt glycogenese een proces dat onmiddellijk na de maaltijd onmiddellijk voorkomt?
- Het ontdekken van de geheimen van hoe chromosomen assembleren
- Waarom leven sommige planten snel en sterven ze jong?
- Drie redenen waarom de celdeling belangrijk is
- Wat zijn drie bronnen van stamcellen?
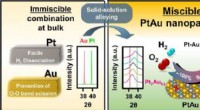
- Directe synthese van waterstofperoxide met een platina-gouden nanodeeltjeskatalysator
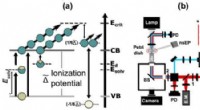
- Geavanceerde computers effent de weg naar de toekomst van NMR-spectroscopie

- Elektrische pulsen gebruiken voor vaccinefficiëntie
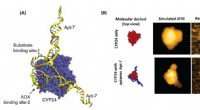
- Veelbelovende antikankermolecuul geïdentificeerd
- De code voor roetvorming kraken - wetenschappers ontrafelen mysterie om gevaarlijke emissies te helpen verminderen

 Bubbeldynamiek onthult hoe je flessen sneller leegt
Bubbeldynamiek onthult hoe je flessen sneller leegt Blootgestelde Chinese database toont diepte van bewakingsstatus
Blootgestelde Chinese database toont diepte van bewakingsstatus Lichaamscamera's hebben mogelijk weinig effect op het gedrag van politie en burgers:studie
Lichaamscamera's hebben mogelijk weinig effect op het gedrag van politie en burgers:studie Welke planten zitten in de maïsfamilie?
Welke planten zitten in de maïsfamilie?  Nieuwe metamaterialen voor het bestuderen van het oudste licht in het universum
Nieuwe metamaterialen voor het bestuderen van het oudste licht in het universum Onderzoek onthult dat ernstige luchtvervuiling de consumptie van voedsel en plastic afval stimuleert
Onderzoek onthult dat ernstige luchtvervuiling de consumptie van voedsel en plastic afval stimuleert ONS, bondgenoten pushen Facebook voor toegang tot versleutelde berichten
ONS, bondgenoten pushen Facebook voor toegang tot versleutelde berichten Hoe Afrika zijn wetenschappelijke onderzoekscapaciteiten heeft ontwikkeld
Hoe Afrika zijn wetenschappelijke onderzoekscapaciteiten heeft ontwikkeld
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

