
Wetenschap
Wat is de elektronenconfiguratie van fluoride?
De elektronenconfiguratie van fluoride (f-) is:
1S² 2S² 2P⁶
Hier komen we daarbij:
* Neutrale fluor (F): Fluor heeft 9 elektronen. De elektronenconfiguratie is 1S² 2S² 2P⁵.
* fluoride-ion (f-): Fluoride krijgt één elektron om een volledig octet te bereiken en stabieler te worden. Dit extra elektron gaat in het 2P -orbitaal.
Daarom is de uiteindelijke elektronenconfiguratie van het fluoride -ion 1S² 2S² 2P⁶.
 Vliegas-geopolymeerbeton:aanzienlijk verbeterde weerstand tegen extreme alkalische aanvallen
Vliegas-geopolymeerbeton:aanzienlijk verbeterde weerstand tegen extreme alkalische aanvallen Waarom komen er dampen vrij als een fles zoutzuur wordt geopend?
Waarom komen er dampen vrij als een fles zoutzuur wordt geopend?  Nieuw gebruik van NMR werpt licht op eenvoudig te maken elektrogepolymeriseerde katalysatoren
Nieuw gebruik van NMR werpt licht op eenvoudig te maken elektrogepolymeriseerde katalysatoren Het aantal mol in een oplossing berekenen
Het aantal mol in een oplossing berekenen Hoe verander je vaste zuurstof in vloeibare zuurstof?
Hoe verander je vaste zuurstof in vloeibare zuurstof?
 Gemeenschappelijke spinnen in Zuid-Texas
Gemeenschappelijke spinnen in Zuid-Texas  Is het tijd om de klimaatbijbel achter zich te laten?
Is het tijd om de klimaatbijbel achter zich te laten?  in Alaska, iedereen worstelt met klimaatverandering
in Alaska, iedereen worstelt met klimaatverandering Brandweerlieden strijden tegen bosbranden in Portugal terwijl de wind aantrekt
Brandweerlieden strijden tegen bosbranden in Portugal terwijl de wind aantrekt Nieuw onderzoek bevestigt dat megabranden niet toenemen:groot, zeer ernstige branden zijn natuurlijk in bossen in het westen van de VS
Nieuw onderzoek bevestigt dat megabranden niet toenemen:groot, zeer ernstige branden zijn natuurlijk in bossen in het westen van de VS
Hoofdlijnen
- Wat hebben andere dieren dat haar?
- Wat zijn concentratiegradiënten in de microbiologie?
- Gentherapie helpt honden met spierdystrofie, mensen daarna?
- Kankerbiologen vinden een sleutel die kan ontsluiten hoe tumoren zich vormen en zich ontwikkelen
- Hoop voor honden met de meest voorkomende hart- en vaatziekten
- Welke mariene dieren of planten beginnen met letters A-Z?
- Hoe een Silly Putty-ingrediënt stamceltherapieën zou kunnen bevorderen
- Een nieuwe kijk op hoe genen zich ontvouwen om hun expressie mogelijk te maken
- Hoe verzamel en analyseer je bacteriën?
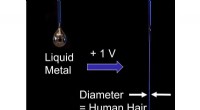
- Beheersing van stromen vloeibaar metaal bij kamertemperatuur
- Ingenieurs 3D printen zeer sterk aluminium, los eeuwenoud lasprobleem op met nanodeeltjes

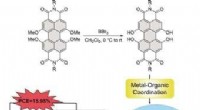
- Organische kleurstof in de tussenlaag van zinkoxide stabiliseert en verbetert de prestaties van organische zonnecellen
- Xenon verbetert de eigenschappen van maxillofaciale en orthopedische implantaten

- Onderzoekers bewijzen dat water meerdere vloeibare toestanden heeft
 Welke chemicaliën zijn schadelijk voor rubberen afdichtingen?
Welke chemicaliën zijn schadelijk voor rubberen afdichtingen?  Esports League begint sterk op ambitieus wereldwijd schema
Esports League begint sterk op ambitieus wereldwijd schema Het sonderen van wateren huid
Het sonderen van wateren huid Nieuwe van der Waals heterostructuren voor zeer efficiënte infrarood fotodetectie
Nieuwe van der Waals heterostructuren voor zeer efficiënte infrarood fotodetectie Heeft Neil Armstrong genoten van de reis naar de maan?
Heeft Neil Armstrong genoten van de reis naar de maan?  Hoeveel elektronen bevinden zich op het buitenste energieniveau van een atoom?
Hoeveel elektronen bevinden zich op het buitenste energieniveau van een atoom?  Welk metaal is in Argentinite?
Welk metaal is in Argentinite?  Wat zijn de eigenschappen van microbiële enzymen?
Wat zijn de eigenschappen van microbiële enzymen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

