
Wetenschap
Heeft stikstof een hoge of lage elektronegativiteit?
Stikstof heeft een relatief hoog elektronegativiteit.
Dit is waarom:
* elektronegativiteit is een maat voor het vermogen van een atoom om elektronen aan te trekken in een chemische binding.
* Stikstof heeft een elektronegativiteitswaarde van 3,04 op de Pauling -schaal.
* Dit is hoger dan veel andere elementen, zoals koolstof (2,55) en waterstof (2.20).
Daarom wordt stikstof als vrij elektronegatief beschouwd. Dit betekent dat het de neiging heeft om elektronen naar zichzelf te trekken in een binding, wat leidt tot polaire covalente bindingen.
 Hoe beïnvloedt elektronisch afval het behoud van de biodiversiteit?
Hoe beïnvloedt elektronisch afval het behoud van de biodiversiteit?  Orkaan Ida treft Louisiana als storm van categorie 4
Orkaan Ida treft Louisiana als storm van categorie 4 Wat is de studie van oorsprong en toekomstig universum genoemd?
Wat is de studie van oorsprong en toekomstig universum genoemd?  Studie:Kunnen de leidende indicatoren van de natuur een milieuramp voorspellen?
Studie:Kunnen de leidende indicatoren van de natuur een milieuramp voorspellen?  CryoSat onthult terugtrekking van Patagonische gletsjers
CryoSat onthult terugtrekking van Patagonische gletsjers
Hoofdlijnen
- Wat werkt het STEM -orgel?
- Welke 2 grote eiwitten die spieren laten bewegen?
- Hoe is een Euglena -achtige plantencelhow het een dierencel?
- Door het proces van meiose worden sekscellen geproduceerd die zijn?
- Chemici, biologen, archeologen:wie zal de recepten van onze voorouders opgraven?
- Waarom is DNA-replicatie belangrijk voor de celcyclus?
- Uw zintuiglijke organen hebben gespecialiseerde cellen genoemd?
- Hoe transcriptiefactoren clusters van specifieke DNA-sequenties vinden en herkennen
- Wat zijn de organismen ontdekt door Jose Rizal?
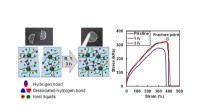
- De toekomst van elektronische apparaten:sterke en zelfherstellende iongels
- Wetenschappers ontdekken pad naar verbetering van baanbrekende batterij-elektrode

- MiNT-eiwit een nieuw doelwit om ziekte aan te vallen
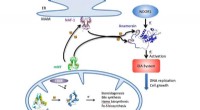
- Osmium-activering in kankercellen

- Diamant uitrekken voor micro-elektronica van de volgende generatie

 Nieuwe analytische techniek helpt onderzoekers subtiele verschillen in subcellulaire chemie op te sporen
Nieuwe analytische techniek helpt onderzoekers subtiele verschillen in subcellulaire chemie op te sporen Geen wondermiddel om het Great Barrier Reef te helpen
Geen wondermiddel om het Great Barrier Reef te helpen Synthese van krachtig antibioticum volgt ongebruikelijke chemische route
Synthese van krachtig antibioticum volgt ongebruikelijke chemische route Leg de relatie uit tussen elektronenorbitalen en energieniveaus?
Leg de relatie uit tussen elektronenorbitalen en energieniveaus?  Leidt 'participatief budgetteren' tot politieke patronage?
Leidt 'participatief budgetteren' tot politieke patronage?  200 miljoen jaar oude insectenkleur onthuld door fossiele schubben
200 miljoen jaar oude insectenkleur onthuld door fossiele schubben Hoe beïnvloeden golven rotsen?
Hoe beïnvloeden golven rotsen?  Wat was het meest zuur?
Wat was het meest zuur?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

