
Wetenschap
Is ICL polaire non of ionisch?
* Elektronegativiteitsverschil: Chloor (CL) is meer elektronegatief dan jodium (I). Dit betekent dat chloor een sterkere trek heeft op de gedeelde elektronen in de binding.
* Polaire covalente binding: Het ongelijke delen van elektronen creëert een gedeeltelijke negatieve lading (Δ-) op het chlooratoom en een gedeeltelijke positieve lading (δ+) op het jodiumatoom.
* Moleculaire geometrie: Het ICL -molecuul heeft een lineaire geometrie. Omdat de ladingen niet symmetrisch zijn, resulteert dit in een netto dipoolmoment, waardoor het molecuul polair wordt.
Samenvattend: Hoewel ICL een aanzienlijk elektronegativiteitsverschil heeft, bereikt het niet de drempel voor een ionische binding. De binding wordt als polair covalent beschouwd, wat resulteert in een polair molecuul.
 Leren van mosselen:een tweekleppige zeedier inspireert onderzoekers om sterkere polymeren te maken
Leren van mosselen:een tweekleppige zeedier inspireert onderzoekers om sterkere polymeren te maken Wat zijn enkele manieren waarop chromatografie chemicaliën in een mengsel kan scheiden?
Wat zijn enkele manieren waarop chromatografie chemicaliën in een mengsel kan scheiden?  Hoe maak je je eigen zonneabsorptiekoeler
Hoe maak je je eigen zonneabsorptiekoeler  Een bliksemsnelle griepvirusdetector
Een bliksemsnelle griepvirusdetector Zou het verbranden van een lucifer een chemische reactie zijn?
Zou het verbranden van een lucifer een chemische reactie zijn?
Hoofdlijnen
- Wat gebeurt er als mitose verkeerd gaat?
- Waar gaat AlphaGo heen?
- Onderzoek laat zien hoe bacteriële ziekteverwekkers zich aanpassen aan voedingsstress
- Het chromosoomnummer in een eiernucleus van een plant is 14 Wat is de normale wortelepidermale dezelfde plant?
- Hoe Charles Darwin werkte
- Op welke manieren kan DNA -mutatie de eigenschappen van een organisme beïnvloeden?
- Wat is de relatie tussen parasiet honingbijen en bijen?
- Hoe verschillen oogenese en spermantogenese?
- Amylase Activity in the Stomach
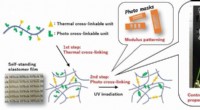
- Films ontwikkelen met instelbare rek en breuk voor verschillende toepassingen
- Onderzoekers ontwikkelen nieuwe membraanloze brandstofcel

- Chemputer belooft app-gestuurde revolutie voor medicijnproductie

- Wetenschappers ontwikkelen een goedkopere methode die kan helpen bij het maken van brandstoffen uit planten

- Wetenschappers ontdekken nieuwe klasse van halfgeleidende entropie-gestabiliseerde materialen

 Welke twee vormen komen prokaryoten binnen?
Welke twee vormen komen prokaryoten binnen?  Heeft H2S een BTU -waarde?
Heeft H2S een BTU -waarde?  Welk eiwit vormt microtubuli in de cel?
Welk eiwit vormt microtubuli in de cel?  Hoe verschilt een maansverduistering van zonne -energie in termen van hun optreden en zichtbaarheid aarde?
Hoe verschilt een maansverduistering van zonne -energie in termen van hun optreden en zichtbaarheid aarde?  Ontgifters van de stortplaats
Ontgifters van de stortplaats Hoe tomatenplanten hun wortels gebruiken om water te rantsoeneren tijdens droogte
Hoe tomatenplanten hun wortels gebruiken om water te rantsoeneren tijdens droogte  Het modelleren van antimicrobieel gebruik en resistentie in Canadese koppels kalkoenen
Het modelleren van antimicrobieel gebruik en resistentie in Canadese koppels kalkoenen China lanceert rover voor eerste andere kant van de maanlanding
China lanceert rover voor eerste andere kant van de maanlanding
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

