
Wetenschap
Wat is de structuur van cesiumchloride?
Key -functies:
* eenheidscel: De eenheidscel van CSCL is een eenvoudige kubus .
* roosterpunten: Er zijn twee roosterpunten per eenheidscel:
* Eén CS⁺ -ion in het midden van de kubus.
* Eén cl⁻ ion in een van de hoeken van de kubus.
* Coördinatienummer: Beide CS⁺- als CL⁻ -ionen hebben een coördinatienummer van 8 . Dit betekent dat elk CS⁺ -ion is omgeven door 8 Cl⁻ -ionen en vice versa.
* stoichiometrie: De eenheidscel weerspiegelt perfect de 1:1 stoichiometrie van CSCL.
Visuele weergave:
U kunt de structuur visualiseren als:
* Een Cl⁻ -ion in het midden van een kubus, met acht CS⁺ -ionen in de hoeken van de kubus.
* Alternatief, stel je een CS⁺ -ion voor in het midden van een kubus met acht Cl⁻ -ionen in de hoeken.
Opmerking: Terwijl de CSCL -structuur naar de verbinding is vernoemd, nemen veel andere ionische verbindingen zoals NaCl bij hoge druk ook deze structuur aan.
Belangrijke overwegingen:
* De CSCL -structuur is alleen stabiel voor ionische verbindingen met een relatief groot kation en een relatief klein anion. Dit komt omdat het grote CS⁺ -ion ruimte nodig heeft om er acht CL⁻ -ionen omheen te huisvesten.
* De CSCL -structuur is een primitief kubisch rooster wat betekent dat er geen atomen in de gezichtscentra van de kubus zijn.
Laat het me weten als je een meer gedetailleerde uitleg wilt van een specifiek aspect van de CSCL -structuur!
 Waarom hooikoorts erger kan worden in een opwarmend klimaat
Waarom hooikoorts erger kan worden in een opwarmend klimaat  Landbouwbranden kunnen de vervuiling in Delhi verdubbelen tijdens het piekseizoen van branden
Landbouwbranden kunnen de vervuiling in Delhi verdubbelen tijdens het piekseizoen van branden Indirecte ontwikkeling versus directe ontwikkeling
Indirecte ontwikkeling versus directe ontwikkeling Hoe verschilt de wetenschap van de wetenschap?
Hoe verschilt de wetenschap van de wetenschap?  Show in Londen verkent de verborgen wereld van gezichtsherkenning
Show in Londen verkent de verborgen wereld van gezichtsherkenning
Hoofdlijnen
- Wat is een groep organen die samenwerken om een specifieke functie te bereiken?
- Hoe vloeistofdynamica en transport de structuur van onze longen vormden tijdens de evolutie
- Denk je dat je een hersenschudding hebt? Een bloedtest kan het diagnosticeren
- Permafrost is kenmerkend voor welk bioom?
- Wat is moleculariteit aan de hand van voorbeelden?
- Wat betekent het woord onafhankelijk in de wetenschap?
- Wie was de vader van taxonomie en hoe classificeerde hij levende organismen?
- Welke twee kenmerken definiëren gymnospermen?
- Wat is een gastplant?
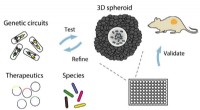
- Onderzoekers ontwikkelen nieuw platform dat kanker in een schaal nabootst om snel de beste bacteriële therapie te bepalen
- Onderzoekers kijken in de databank van waterclusters, treinnetwerk om energielandschappen te voorspellen

- De eigenschappen van composieten voor het bouwen van betrouwbare treinen

- Plastic afval omzetten in smeeroliën
- Ontwerpen van het perfecte membraan voor schone scheiding van gassen

 Naar een circulaire economie:Europese fabrikanten hebben de neiging om niet te rapporteren over hun acties
Naar een circulaire economie:Europese fabrikanten hebben de neiging om niet te rapporteren over hun acties Geologisch bewijs is de voorloper van onheilspellende vooruitzichten voor een opwarmende aarde
Geologisch bewijs is de voorloper van onheilspellende vooruitzichten voor een opwarmende aarde Hoe kweekhuizen werken
Hoe kweekhuizen werken  Een stof die kan worden gescheiden is een?
Een stof die kan worden gescheiden is een?  Team ontdekt de relatie tussen de timing van DNA-replicatie en hoe genen zich vouwen in 3D-structuren in de celkern
Team ontdekt de relatie tussen de timing van DNA-replicatie en hoe genen zich vouwen in 3D-structuren in de celkern  Verminderde energie van de zon zou tegen het midden van de eeuw kunnen optreden - nu, wetenschappers weten door hoeveel
Verminderde energie van de zon zou tegen het midden van de eeuw kunnen optreden - nu, wetenschappers weten door hoeveel Nieuw inzicht in waarom de ziekte van Pierce zo dodelijk is voor wijnstokken
Nieuw inzicht in waarom de ziekte van Pierce zo dodelijk is voor wijnstokken  Uitbreidbare nanodeeltjes zijn veelbelovend bij de behandeling van dodelijke buikholtetumoren
Uitbreidbare nanodeeltjes zijn veelbelovend bij de behandeling van dodelijke buikholtetumoren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

