
Wetenschap
Waarom geven natriumchloride en de oplossingen van nitraat allemaal dezelfde kleurvlam aan?
* Elektronische excitatie: Wanneer een verbinding die natrium bevat, in een vlam wordt verwarmd, absorberen de elektronen in de natriumatomen energie en springen ze naar hogere energieniveaus (geëxciteerde toestand).
* Emissie van licht: Terwijl deze opgewonden elektronen terugkeren naar hun grondtoestand, geven ze de geabsorbeerde energie als licht vrij. De golflengte van dit uitgezonden licht komt overeen met de oranje-gele kleur die we zien.
* Natriumdominantie: Natriumionen zijn zeer efficiënt in het uitzenden van dit oranje geel licht. Dit betekent dat zelfs als andere elementen aanwezig zijn, de sterke emissie van het natrium de neiging heeft om de vlamkleur te domineren.
* nitraat en natrium: Hoewel nitraten zelf niet direct bijdragen aan de kleur, bevatten ze vaak natrium als een tegenion (bijvoorbeeld natriumnitraat, nano₃). Wanneer verwarmd, worden de natriumionen vrijgegeven en vertonen ze hun karakteristieke vlamkleur.
Key Takeaway: De oranje geelle vlamkleur is voornamelijk te wijten aan de aanwezigheid van natriumionen, ongeacht de specifieke verbinding die ze bevat.
 Wat maakt invloedrijke wetenschap? Een goed verhaal vertellen
Wat maakt invloedrijke wetenschap? Een goed verhaal vertellen  Recycle anesthetica om de CO2-uitstoot van de gezondheidszorg te verminderen, studie concludeert
Recycle anesthetica om de CO2-uitstoot van de gezondheidszorg te verminderen, studie concludeert Wat zijn de parkregels in Uluru Kata Tjuta National Park?
Wat zijn de parkregels in Uluru Kata Tjuta National Park?  Machine learning identificeert verbanden tussen de oceanen van de wereld
Machine learning identificeert verbanden tussen de oceanen van de wereld Everglades herstel moet omgaan met stijgende oceaan, nieuw rapport zegt:
Everglades herstel moet omgaan met stijgende oceaan, nieuw rapport zegt:
Hoofdlijnen
- Flashmob in de kern:studie maakt duidelijk waarom sommige eiwitten 'samenkomen'
- Wat is de rol van bromofenol blauw plasmide -DNA -isolatie?
- Onderzoeken hoe gemodificeerde genen de natuur in ontsnappen
- Wat zijn enkele omgevingsfactoren die de zaadkieming kunnen bevorderen?
- Wie zijn de drie auteurs van de celtheorie?
- Wat zijn voorbeelden van wetenschappelijke conclusies?
- Nucleïnezuren waar bevinden ze zich in uw lichaam?
- Marine fytoplankton redt zich met een beetje hulp van zijn bacterievrienden
- Steur blijft zeldzaam in de Grote Meren, maar de bevolking van Detroit Rivers bloeit
- Nieuwe structurele details over de specifieke rangschikking van atomen in geconjugeerde polymeren
- Geuren langer laten duren

- Oplossingsverwerkte OLED's maken de weg vrij voor toekomstige verlichtingstoepassingen

- Generatie van een stabiel biradicaal
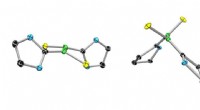
- Wetenschappers stellen een dynamische ladings- en oxidatietoestand voor voor katalysatoren met één atoom
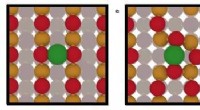
 Controle over de Amerikaanse senaat:wat leert de geschiedenis ons over de mate waarin het de wetgevende beleidsvorming beïnvloedt?
Controle over de Amerikaanse senaat:wat leert de geschiedenis ons over de mate waarin het de wetgevende beleidsvorming beïnvloedt? Is het bevrijden van een chemische of fysieke verandering?
Is het bevrijden van een chemische of fysieke verandering?  EU-hof steunt Frankrijk verbod op Uber-service zonder Brussel op de hoogte te stellen
EU-hof steunt Frankrijk verbod op Uber-service zonder Brussel op de hoogte te stellen Is the Betelgeuse and stars different colors?
Is the Betelgeuse and stars different colors?  Hoe kwamen planten zonlicht in energie?
Hoe kwamen planten zonlicht in energie?  Voedselwetenschappers tonen aan dat rijstmout potentieel een grotere rol kan spelen in bier
Voedselwetenschappers tonen aan dat rijstmout potentieel een grotere rol kan spelen in bier  Hoe werkt het C4 -pad?
Hoe werkt het C4 -pad?  Pangolins in Africa:Expert legt uit waarom miljoenen illegaal zijn verhandeld en wat eraan kan worden gedaan
Pangolins in Africa:Expert legt uit waarom miljoenen illegaal zijn verhandeld en wat eraan kan worden gedaan
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

